Subiecte:
- introducere
- Proces circular
- Înregistrează diagrama ph
- Comparați R134a cu R1234yf
Introducere:
Procesul de răcire din aerul condiționat al unei mașini folosește modificări ale stării unei substanțe. În timpul unei schimbări de stare, cum ar fi trecerea de la lichid la vapori, structura moleculară a substanței se modifică, ceea ce necesită căldură. Căldura este absorbită atunci când lichidul se transformă în vapori, iar în cazul opus, la trecerea de la vapori la lichid, căldura este eliberată.
Dacă ne uităm la transferul de căldură către și dinspre mediu, vedem că în timpul procesului de evaporare mediul se răcește, în timp ce căldură este eliberată și mediul se încălzește în timpul condensului. Această răcire a mediului are loc în evaporator, în timp ce încălzirea are loc în condensator. Acest proces se repetă continuu, motiv pentru care este cunoscut ca proces circular.
Pe pagina „Introducere aer condiționat”, procesul ciclului cu diferitele componente ale aerului condiționat este descris într-o manieră practică. Pe această pagină vom aprofunda în continuare acest proces ciclului prin diagrama log pH.
Proces de reciclare:
Înainte de a arăta un diagramă complet de log pH, să începem cu procesul ciclului de aer condiționat. În acest proces de ciclu folosim diagrama agentului frigorific R134a. În această diagramă, zonele pentru gaz, gaz-lichid și lichid se disting unele de altele. Punctul critic este în vârf, la 101 grade Celsius și o presiune de 40 bar. Acestea sunt temperatura și presiunea maximă la care agentul frigorific este stabil din punct de vedere chimic. Conținutul de căldură (entalpia) este reprezentat grafic în funcție de presiunea de pe axa x. Deși adesea ne referim la el ca o „diagramă pH”, este de fapt o „diagramă log-pH” din cauza scalarii logaritmice.
- La punctul 1 din diagramă pornește compresorul, care atrage agentul frigorific din evaporator. Presiunea este de 2 bar;
- Gazul este comprimat de la 1 la 2, crescând presiunea și conținutul de căldură. Presiunea și temperatura cresc la 15 bar și 70 de grade Celsius. Gazul este supraîncălzit;
- Datorită degajării de căldură în condensator, conținutul de căldură scade și deci inițial temperatura. Gazul își pierde supraîncălzirea între punctele 2 și 3, determinând o scădere a temperaturii de la 70 la 55 ° C
- De la punctul 3 la 4 există eliberare de căldură la o temperatură constantă. Aici gazul este transformat în lichid. Presiunea rămâne constantă;
- Răcirea ulterioară face ca lichidul să devină ușor suprarăcit (de la 4 la 5). Lichidul suprarăcit sub presiunea mare de 15 bar ajunge la o constricție în punctul 5: supapa capilară sau de expansiune. Aici presiunea mare este separată de presiunea joasă. De la compresor mai putem spune ca presiunea de refulare este separata de presiunea de aspiratie.
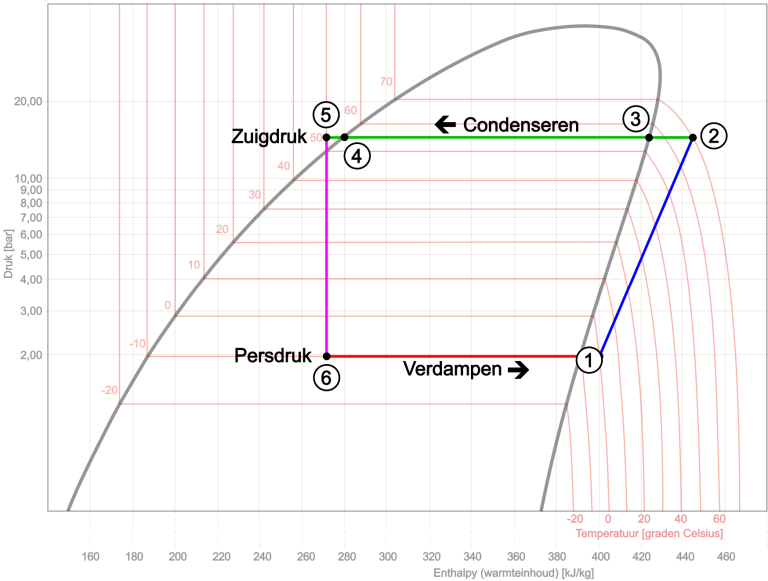
Datorită scăderii bruște a presiunii în constricție, punctul de fierbere al agentului frigorific în faza lichidă va scădea, determinând evaporarea spontană. Căldura necesară pentru aceasta este mai întâi extrasă din agentul frigorific în sine și din împrejurimile acestuia. Aceasta rămâne conținutul de căldură este aproape constant. Evaporarea completă are loc apoi în evaporator de la punctul 6 la 1. Temperatura de fierbere a agentului frigorific scade între punctele 5 și 6 din 50° C până la -10°C, în cele din urmă încălzindu-se până la punctul 1 ca gaz până la 0°C. Conținutul de căldură al agentului frigorific crește, căldura necesară fiind extrasă din mediu, în acest caz aerul care trece prin evaporator. Presiunea și temperatura rămân practic constante. Agentul frigorific părăsește vaporizatorul sub formă de vapori și este aspirat din nou de compresor în punctul 1. Procesul se repetă.
Diagrama log pH:
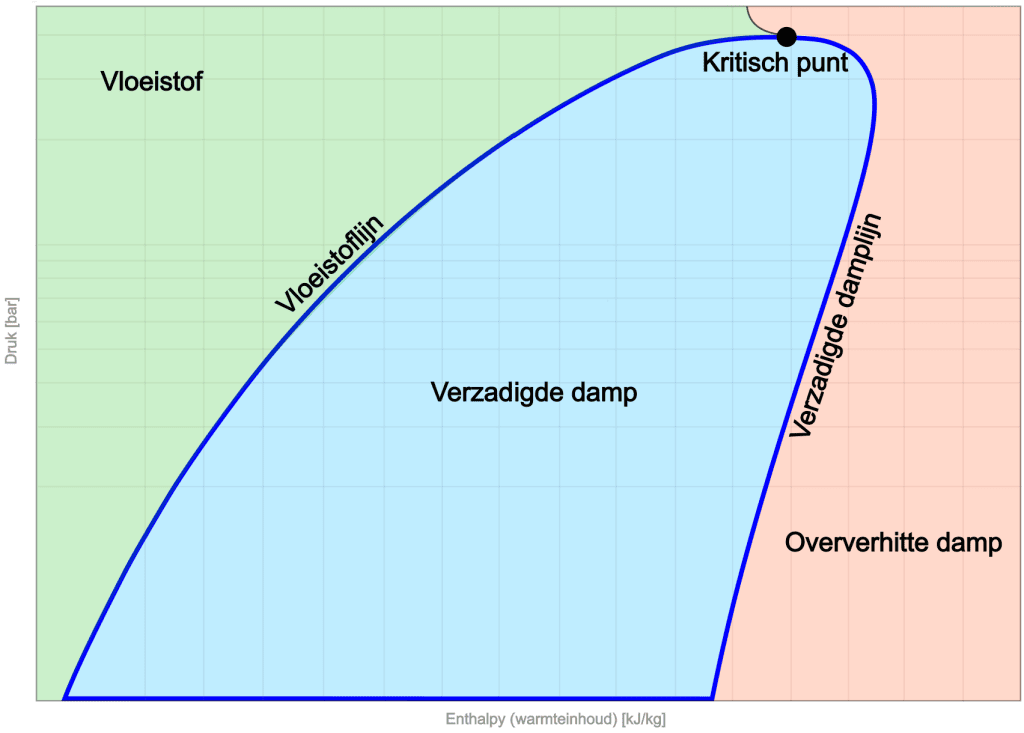
În secțiunea anterioară, a fost prezentată diagrama log pH care arată procesul ciclului (de la evaporare la condensarea agentului frigorific. Imaginea de mai jos arată starea agentului frigorific la o anumită presiune în raport cu entalpia (conținutul de căldură), în care procesul de ciclizare este indicat de linia albastră închisă.
În partea stângă a diagramei este zona fluidului. La entalpie scăzută, agentul frigorific este sub formă lichidă. Odată cu creșterea entalpiei, se ajunge la linia lichidului. Panta acestei linii indică modificările de presiune și de entalpie pentru faza lichidă.
În centrul diagramei se află zona de vapori saturați. Aici agentul frigorific este în echilibru termic, cu atât lichid, cât și vapori prezenți.
În dreapta vedem linia de vapori saturați, care marchează limita la care agentul frigorific s-a evaporat complet și se află într-o fază de vapori supraîncălziți.
În partea de sus a diagramei se află punctul critic, care marchează granița dintre lichid și vapori. Aici dispare distincția dintre faza de vapori și cea lichidă, lăsând agentul frigorific într-o stare unică. Nu există o tranziție clară între lichid și vapori.
Pentru a oferi mai multe informații asupra diagramei log-ph, mai multe curbe sunt adăugate diagramei de mai jos: calitatea izoentropică, izotermă, izocorică și a vaporilor. În desenul de mai jos vedem din nou procesul circular (colorat gri) cu progresia celorlalte procese. Iată o scurtă explicație a fiecărei schimbări de stare:
Isentropic: linia isentropică și este caracterizată de entropie constantă. Aceasta înseamnă că, în timpul unui proces de-a lungul acestei linii, agentul frigorific nu are schimb de căldură cu mediul și nu suferă nicio modificare a entropiei. Este o linie de proces adiabatică (fără schimb de căldură) eficientă din diagramă.
Izotermă: O linie izotermă din diagrama log-pH reprezintă un proces de temperatură constantă. În timpul acestui proces, temperatura agentului frigorific rămâne constantă, ceea ce înseamnă că căldura este furnizată sau îndepărtată pentru a menține constant raportul presiune-entalpie (ph).
Isocor: O linie izocorică în diagrama log-pH reprezintă un proces de volum constant. În timpul acestui proces, volumul specific al agentului frigorific rămâne constant, ceea ce înseamnă că nu are loc nicio modificare a volumului. Acest lucru permite stilului de linie să se miște în sus sau în jos în diagramă, în funcție de alte modificări, cum ar fi presiunea și entalpia.
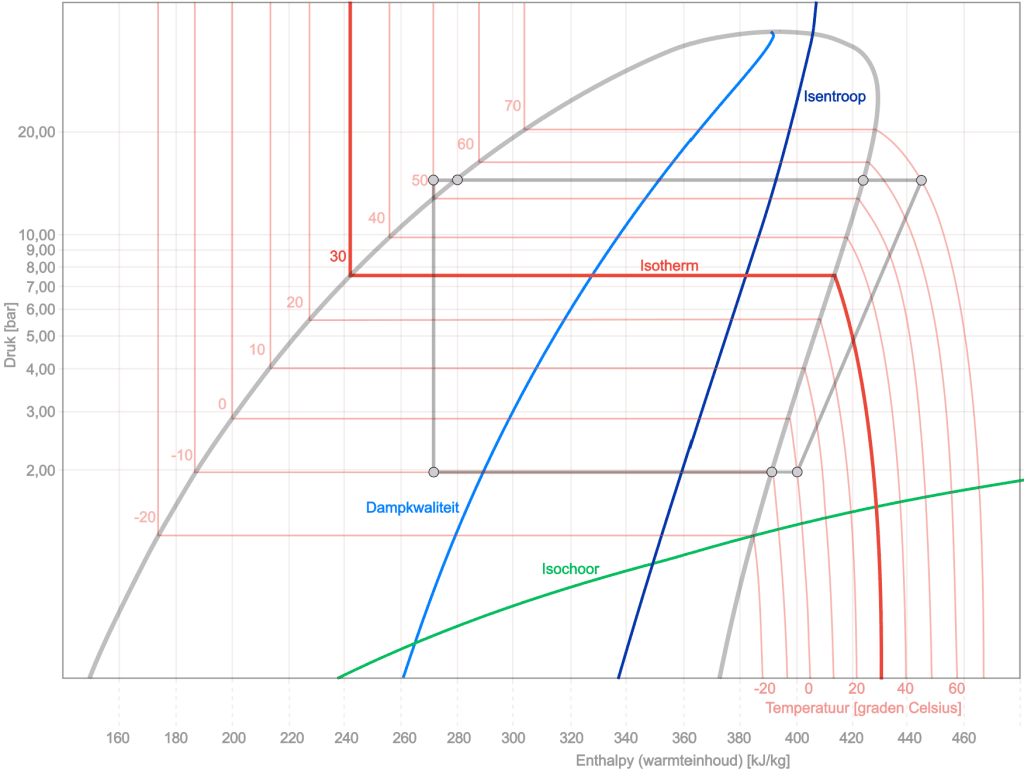
- Calitatea vaporilor: Într-o diagramă a pH-ului agentului frigorific, axa x indică domeniul de calitate, de la „x=0” (complet lichid) la „x=1” (complet gazos). Între aceste extreme, agentul frigorific este într-o stare în două faze, valoarea x indicând raportul dintre gaz și lichid. O linie de la „x=0,10” la „x=0,90” în diagramă indică faptul că agentul frigorific se află în acest interval bifazic, valoarea x specifică indicând partiția gaz/lichid. Acest lucru este crucial pentru înțelegerea comportamentului agentului frigorific în aplicații precum sistemele de refrigerare și aer condiționat.
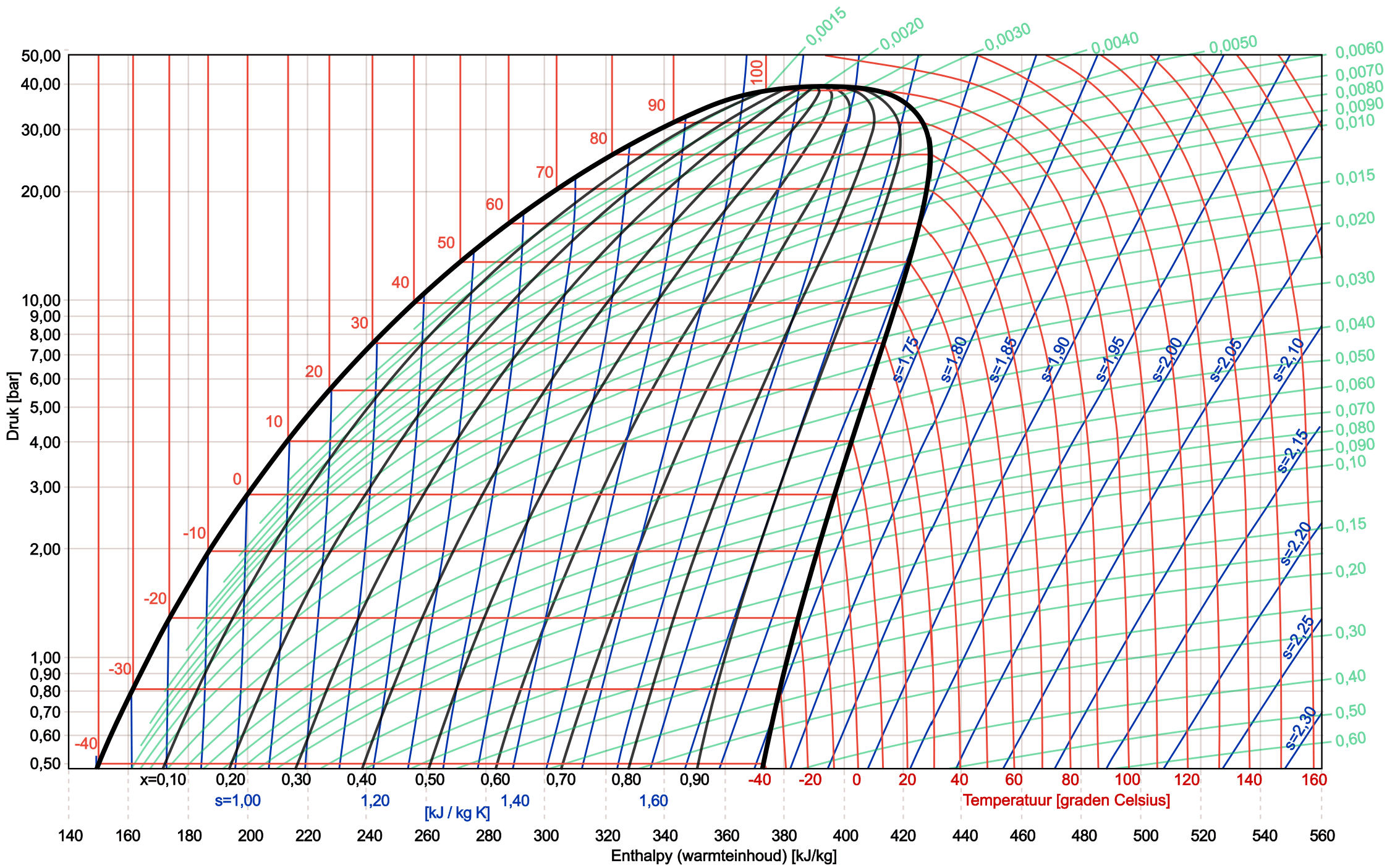
În imaginea de mai jos vedem o diagramă log pH completă a agentului frigorific R134a.
Comparați R134a cu R1234yf:
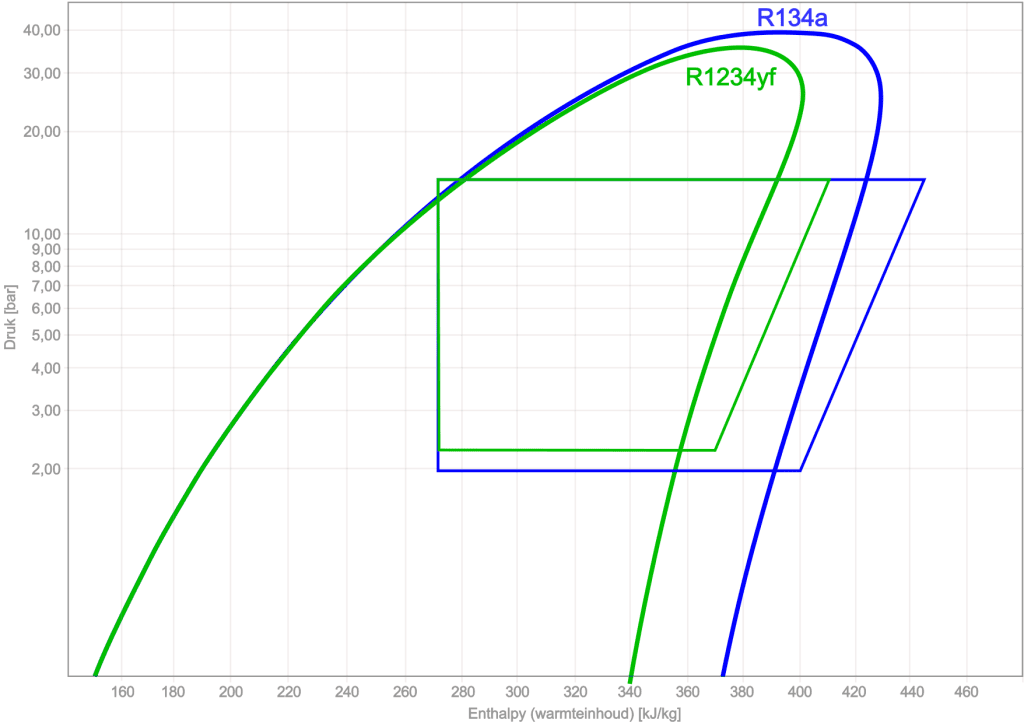
Folosind diagrama log pH, diferite tipuri de agenți frigorifici pot fi comparate între ele. Următoarea figură prezintă diagramele log pH și procesele de ciclu ale R134a și R1234yf.
Pagina înrudită:
