Emner:
- hydrogen
- Produksjon av hydrogen
- Hydrogen som drivstoff for en Otto-motor
- Brenselcelle
- Oppbevaringstank
- Rekkevidde og kostnader for hydrogen
Hydrogen:
Hydrogen (kalt hydrogen på engelsk) kan brukes som energibærer for å drive kjøretøy. Energibærer betyr at energi allerede er lagt inn i hydrogenet på forhånd. Dette i motsetning til (fossile) energikilder som olje, naturgass og kull, hvor energien hentes ved å bearbeide disse stoffene ved å brenne dem.
Hydrogen er derfor noe helt annet enn vanninjeksjon, som ikke brukes som energibærer i bensinmotorer, men rent for å kjøle ned forbrenningskammeret.
Målet er å oppnå «nullutslipp» med hydrogen; en energiform som ikke produserer skadelige gasser under bruk. Overgangen fra fossilt brensel til elektrisk fremdrift i kombinasjon med hydrogen og en brenselcelle faller inn under energiovergang. Å drive kjøretøy med hydrogen kan gjøres på to forskjellige måter:
- Bruker hydrogen som drivstoff for Otto-motoren. Hydrogenet erstatter bensindrivstoffet.
- Generer elektrisk energi ved hjelp av hydrogen i en brenselcelle. Ved å bruke denne elektriske energien vil den elektriske motoren drive kjøretøyet helt elektrisk.
Begge teknikkene er beskrevet på denne siden.
Hydrogen kan produseres med bærekraftig energi eller basert på fossilt brensel. Vi prøver å forhindre det siste så mye som mulig, fordi fossilt brensel vil bli mangelvare i fremtiden. CO2 vil også bli produsert ved prosessering av fossilt brensel.

Kolonnene under viser energiinnholdet i et batteri, hydrogen og bensin. Vi ser at det er mye
Batteri:
- Energiinnhold: 220Wh/kg, 360 Wh/l
- Veldig effektiv
- Kort oppbevaring
- Direkte energifrigjøring mulig
- Transport er komplisert
Hydrogen (700 bar):
- Energiinnhold: 125.000 kJ/kg, 34,72 kWh/kg
- 30 % varme, 70 % H2 (PEM brenselcelle)
- Lang lagring mulig
- Konvertering nødvendig
- Transportvennlig
Bensin:
- Energiverdi: 43.000 kJ/kg, 11,94 kWh/kh
- Avkastning opptil 33 %
- Lang lagring mulig
- Ombygging nødvendig (forbrenning)
- Transportvennlig
Hydrogen finnes overalt rundt oss, men aldri gratis. Det er alltid bundet. Vi skal produsere det, isolere det og lagre det.
- 1 kg ren hydrogengass (H2) = 11.200 XNUMX liter ved atmosfærisk trykk
- H2 er mindre enn noe annet molekyl
- H2 er lettere enn noe annet molekyl
- H2 leter alltid etter forbindelser
I tillegg til produksjon og bruk av hydrogen i personbiler, diskuterer denne siden også lagring og transport av hydrogen (nederst på siden).
Produksjon av hydrogen:
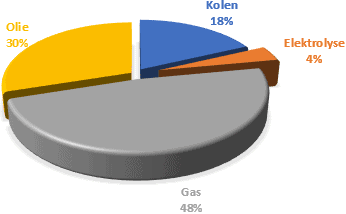
Hydrogen er en gass som ikke utvinnes fra bakken, som naturgass. Hydrogen må produseres. Dette gjøres blant annet gjennom elektrolyse, en prosess der vann omdannes til hydrogen og oksygen. Det er det motsatte av reaksjonen som finner sted i en brenselcelle. I tillegg kan hydrogen fås gjennom mindre miljøvennlige prosesser. Dataene nedenfor viser hvordan hydrogen kan produseres i 2021.
- Kull: C + H20 -> CO2 + H2 + Nox + SO2 + … (temp: 1300C-1500C)
- Naturgass: CH4 + H2O -> CO2 + 3H2 (nødvendig temp: 700C-1100C)
- Olje: CxHyNzOaSb + …. -> cH2 + veldig mange biprodukter
- Elektrolyse fra vann: 2H2O -> 2H2 + O2
Elektrolyse fra vann er veldig rent og er den mest miljøvennlige formen for hydrogenproduksjon. Dette frigjør hydrogen og oksygen, i motsetning til prosessering av fossilt brensel, som frigjør CO2.
- Elektrolyse av vann; Elektrolyse er en kjemisk reaksjon som deler vannmolekyler for å lage rent hydrogen og oksygen. Hydrogen kan lages overalt hvor det er vann og strøm. En ulempe er at man trenger strøm for å lage hydrogen for så å gjøre det om til strøm igjen. Opptil 50 % går tapt under denne prosessen. Fordelen er at energien er lagret i hydrogen.
- Konvertering av fossilt brensel; olje og gass inneholder hydrokarbonmolekyler som består av karbon og hydrogen. Hydrogen kan spaltes fra karbon ved hjelp av en såkalt drivstoffprosessor. Ulempen er at karbonet forsvinner ut i luften som karbondioksid.
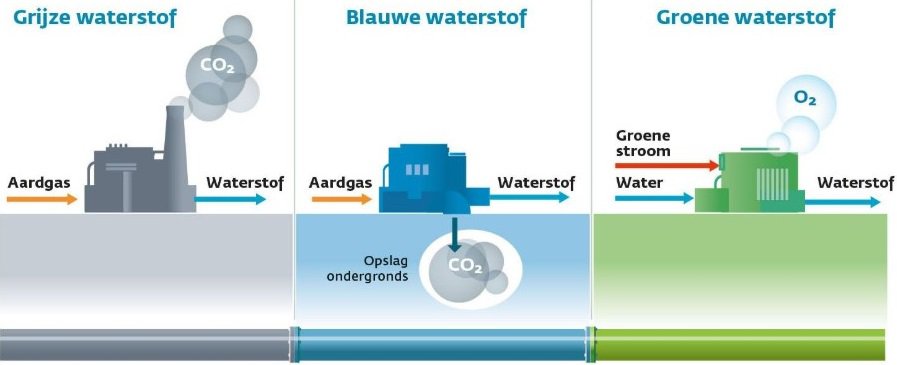
Hydrogenproduksjonen som oppnås med fossilt brensel kalles grå hydrogen. Dette frigjør NOx og CO2 til atmosfæren.
Fra 2020 og utover vil produksjonen bli stadig mer «blå»: CO2 skal fanges.
Målet er å produsere utelukkende grønt hydrogen innen 2030: grønn strøm og vann er kildene til det mest miljøvennlige hydrogenet som produseres.
I den kjemiske verden omtales hydrogen som H2, som betyr at et hydrogenmolekyl består av to hydrogenatomer. H2 er en gass som ikke forekommer i naturen. H2-molekylet forekommer i alle slags stoffer, det mest kjente er vann (H20). Hydrogen må fås ved å skille hydrogenmolekylet fra for eksempel et vannmolekyl.
Å produsere hydrogen gjennom elektrolyse er derfor fremtiden.
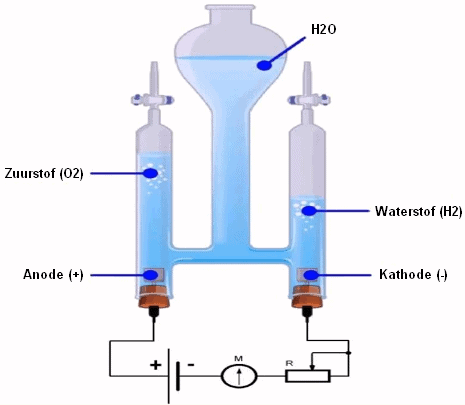
Følgende bilde viser en modell som vanligvis brukes i kjemitimer.
- Positive og negative stolper på et batteri henger i vannet;
- På anodesiden får du oksygen;
- På katodesiden får du hydrogen.
Hydrogen produsert fra fossilt brensel, for eksempel Metan (CH4), blir i dette tilfellet omdannet til H2 og CO2 via reformering. CO2en kan separeres og lagres under bakken, for eksempel i et tomt naturgassfelt. Bruk av naturgass gir derfor lite eller ingen bidrag til CO2-utslipp til atmosfæren. Hydrogen kan også lages av biomasse. Dersom CO2 som frigjøres under denne prosessen også separeres og lagres under bakken, er det til og med mulig å oppnå negative CO2-utslipp; fjerne CO2 fra atmosfæren og lagre denne CO2 på jorden.
Hydrogen er, i motsetning til fossilt brensel som olje, naturgass og kull, ikke en energikilde, men en energibærer. Det betyr at energien som frigjøres ved bruk av hydrogen, for eksempel som drivstoff i en bil, først må inn. Elektrisitet er nødvendig for å produsere hydrogen gjennom elektrolyse. Bærekraften til dette hydrogenet avhenger da i stor grad av bærekraften til elektrisiteten som brukes.
Hydrogen som drivstoff for en Otto-motor:
En Otto-motor er et annet navn for en bensinmotor. Bensinmotoren ble oppfunnet i 1876 av Nikolaus Otto. I dette tilfellet kaller vi det en Otto-motor, fordi bensinen erstattes av et annet drivstoff, nemlig hydrogen. I en motor hvor hydrogen sprøytes inn, er det ikke lenger en drivstofftank med bensin.
Når hydrogen brennes, produseres det ikke CO2-gasser, i motsetning til konvensjonelle Otto- og dieselmotorer, men kun vann. Når hydrogen injiseres via direkte injeksjon, vil det være en effektøkning på 15 til 17 % sammenlignet med bensin. Når hydrogenet injiseres inn i innløpsventilen (indirekte injeksjon), skjer rask oppvarming gjennom luften. Luften fortrenges også av hydrogenet. I begge tilfeller strømmer mindre oksygen (O2) inn i brennkammeret. I verste fall er det et effekttap på opptil 50 %.
Forholdet mellom luft og hydrogen er ikke så nøyaktig som for eksempel en luft-bensinblanding. Formen på brennkammeret er derfor ikke av stor betydning.
Hydrogen kan injiseres på to måter:
– Væske: Ved væsketilførsel av hydrogen vil forbrenningstemperaturen synke relativt på grunn av fordampning, slik at det dannes mindre NOx.
– Gassformig: Dersom hydrogenet er lagret i flytende form i tanken og det strømmer inn i forbrenningsrommet ved omgivelsestemperatur, må det brukes en fordamper for å omdanne hydrogenet fra flytende til gassform. I så fall varmes fordamperen opp av motorkjølevæsken. Mulige tiltak for å redusere NOx er; søker EGR, vanninjeksjon eller en lavere kompresjonsforhold.
Bildet nedenfor viser fire situasjoner med tre forskjellige versjoner av hydrogeninjeksjon. På det andre bildet fra venstre injiseres det gassformige hydrogenet indirekte inn i inntaksmanifolden. Det gassformige hydrogenet varmes opp av omgivelsestemperaturen. Hydrogenet tar også opp plass, og får mindre oksygen til å strømme inn i sylinderen. Dette er situasjonen der det oppstår mest krafttapet.
På det tredje bildet tilføres hydrogenet i flytende form. Kryogen betyr at hydrogenet har blitt avkjølt veldig kraftig (en metode for å lagre store mengder hydrogen i flytende form i en relativt liten lagertank). Fordi temperaturen på hydrogenet er lavere og det er i flytende tilstand, skjer det bedre sylinderfylling. På grunn av den lave temperaturen oppnås en virkningsgrad nesten like høy som en motor med direkte (hydrogen)innsprøytning. Direkteinnsprøytningsmotoren kan sees på det fjerde bildet. Hele forbrenningsrommet er fylt med oksygen. Når inntaksventilen er stengt og stemplet komprimerer luften, injiseres en viss mengde hydrogen gjennom injektoren. Tennpluggen på denne motoren er bak eller ved siden av injektoren (dette er ikke vist på bildet).
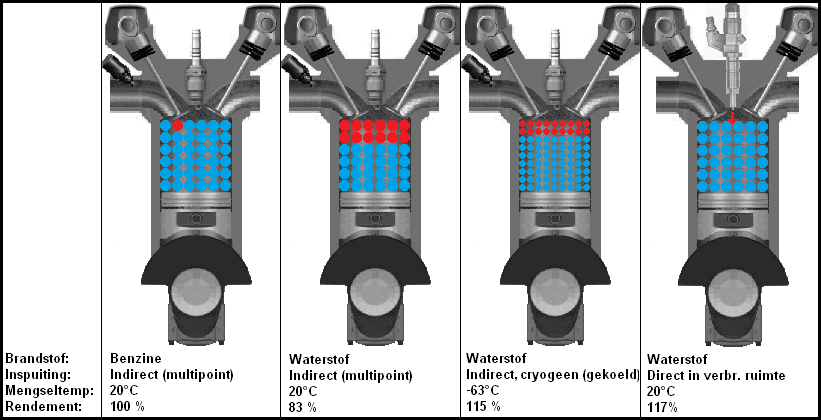
Effektiviteten til en Otto-motor er selvfølgelig ikke 100 %, men i dette bildet sammenlignes effektiviteten ved forbrenning av hydrogen med forbrenning av bensin.
Hydrogen har en høy energitetthet per masseenhet (120MJ/kg), noe som gjør den nesten tre ganger så høy som bensin. De gode tenningsegenskapene til hydrogen gjør det mulig å kjøre motoren svært mager, med en lambdaverdi på 4 til 5. Ulempen med å bruke en mager blanding er at effekten blir lavere og kjøreegenskapene reduseres. For å kompensere for dette brukes ofte superlading (en turbo).
På grunn av det større tenningsområdet sammenlignet med bensin, er risikoen for detonasjon eller tilbakeslag større. Det er derfor svært viktig at det er god kontroll på drivstofftilførsel og tenning. Ved full belastning kan temperaturen i brennkammeret bli svært høy. Det er ofte vanninjeksjon nødvendig for å sikre tilstrekkelig kjøling og dermed forhindre for tidlig antennelse (i form av detonasjon eller tilbakeslag).
Brenselcelle:
Den forrige delen forklarte hvordan hydrogen kan tjene som drivstoff for forbrenningsmotoren. En annen anvendelse av hydrogen er i brenselcellen. Et kjøretøy utstyrt med brenselcelle har ikke en forbrenningsmotor, men en eller flere elektriske motorer. Den elektriske energien for å drive de elektriske motorene produseres av brenselcellen. En brenselcelle er en elektrokjemisk enhet som konverterer kjemisk energi direkte til elektrisk energi, uten termiske eller mekaniske tap. Energiomsetningen i brenselcellen er derfor svært effektiv. Brenselcellen går generelt på hydrogen, men et drivstoff som metanol kan også brukes.
En brenselcelle kan i prinsippet sammenlignes med et batteri, fordi begge produserer strøm gjennom en kjemisk prosess. Forskjellen er at den lagrede energien i batteriet frigjøres én gang. Energien går tom over tid, så batteriet må lades. En brenselcelle gir kontinuerlig energi, så lenge reaktanter tilføres den elektrokjemiske cellen. Reaktanter er kjemiske stoffer som reagerer med hverandre i en kjemisk reaksjon.
I en brenselcelle omdannes hydrogen og oksygen til H+ og OH- ioner (ladede partikler). Ionene separeres med en membran i separate kamre i brenselcellen. Brenselcellen inneholder to porøse karbonelektroder som en katalysator påføres på; for hydrogen (H) en negativ elektrode (anode) og for oksygen (O) en positiv elektrode (katode).
H+ og OH- ioner ledes til hverandre via elektrodene (anode og katode), hvoretter + og – ionene reagerer med hverandre. Katoden katalyserer reaksjonen der elektronene og protonene reagerer med oksygen for å danne sluttprodukt to, nemlig vann. H+- og OH-ionene danner sammen et H2O-molekyl. Dette molekylet er ikke et ion fordi dets elektriske ladning er nøytral. Plusspartikkelen og minuspartikkelen gir sammen en nøytral partikkel.
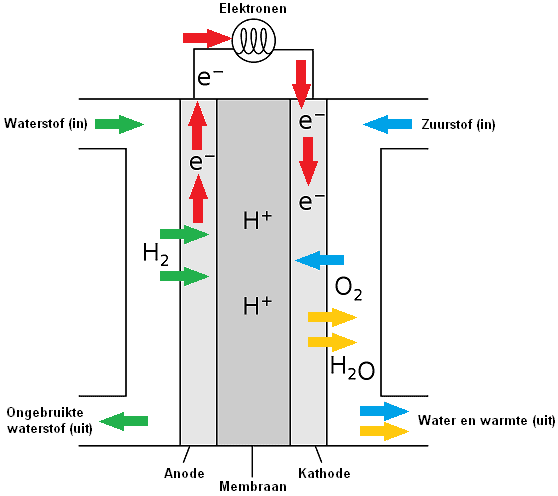
Oksydasjonen av hydrogen (H) skjer ved anoden. Oksidasjon er prosessen der et molekyl donerer elektronene sine. Anoden fungerer som en katalysator, og deler hydrogenet i protoner og elektroner.
Reduksjon skjer ved katoden ved å tilsette oksygen (O). Elektronene, forseglet av anoden, vil reise til katoden via en elektrisk ledning som forbinder elektronene rundt utsiden.
Ved å ikke overføre elektroner direkte, men via en ekstern rute (strømledningen), frigjøres denne energien i stor grad som elektrisk energi. Kretsen er lukket av ioner i en forbindelseselektrolytt mellom reduksjonsmiddel og oksidasjonsmiddel.
Partikkelen som absorberer elektroner kalles et oksidasjonsmiddel og reduseres derved. Reduksjonsmidlet mister elektroner og oksideres. En reduksjon er prosessen der en partikkel absorberer elektroner. Oksidasjon og reduksjon går alltid sammen. Antall elektroner som frigjøres og absorberes er alltid det samme.
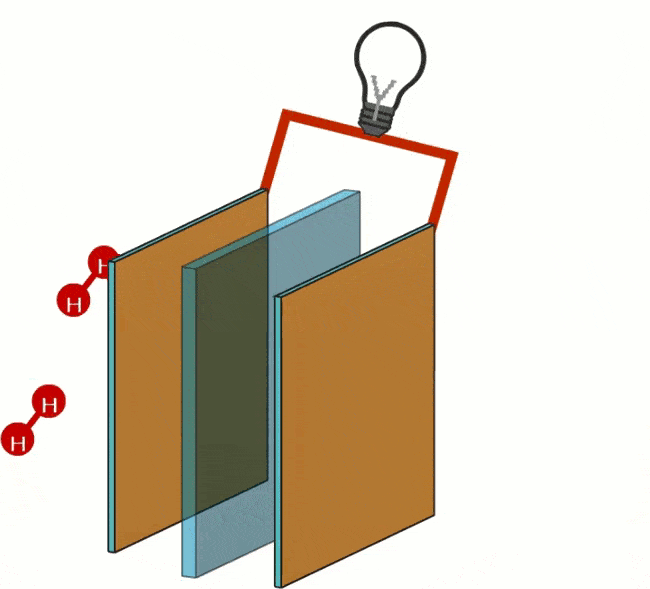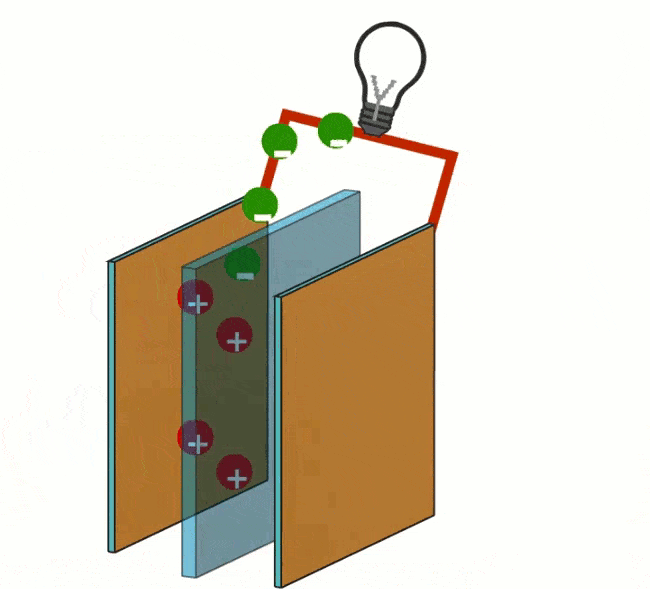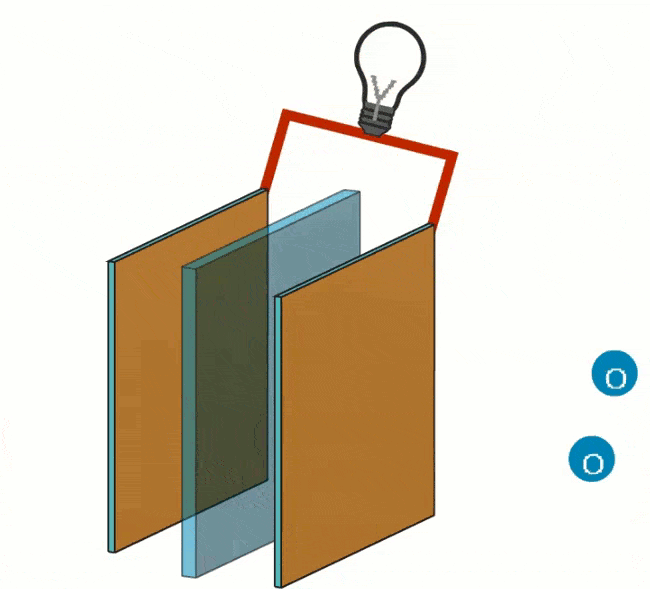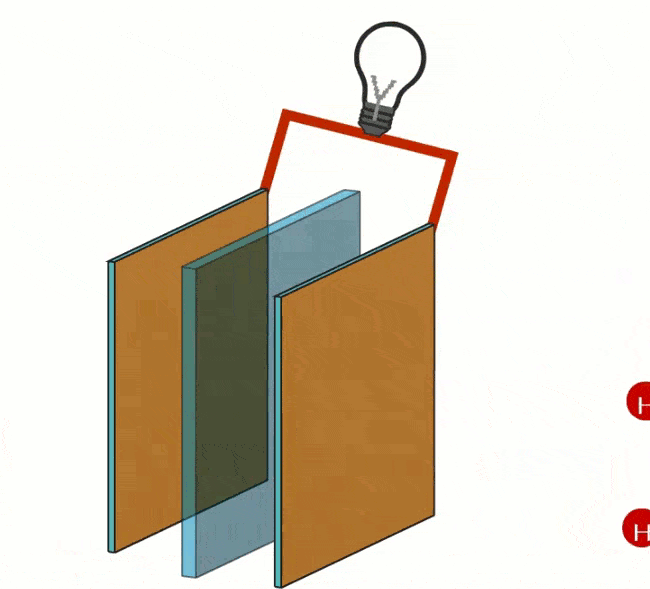
Følgende reaksjon finner sted ved minuspolen:
En annen reaksjon finner sted ved den positive polen:
Bildet nedenfor viser bunnen av en Toyota brenselcellestabel. Denne brenselcellestabelen er plassert under panseret på bilen. Den elektriske motoren er festet til denne stabelen. Den elektriske motoren leverer kraften til transmisjonen, som er koblet til drivakslene for å overføre drivkreftene til hjulene.
Flere luftrør kan sees på toppen av stabelen. Dette inkluderer blant annet luftpumpen som pumper luften til brenselcellene, avhengig av kraften som kreves av elmotoren.
Denne brenselcellestabelen er utstyrt med 370 brenselceller. Hver brenselcelle leverer 1 volt, så totalt kan det tilføres 370 volt til elmotoren. Alle brenselcellene er plassert under hverandre. Den røde sirkelen viser en forstørrelse, hvor stablingen av brenselcellene tydelig kan sees.

Oppbevaringstank:
Selv om hydrogen har en høy energitetthet per masseenhet (120MJ/kg) og derfor er nesten tre ganger så høy som bensin, er energitettheten per volumenhet svært lav på grunn av dens lavere spesifikke masse. For lagring betyr dette at hydrogenet må lagres under trykk eller i flytende form for å kunne bruke en lagertank med håndterlig volum. Det er to varianter for kjøretøyapplikasjoner:
- Gasslagring ved 350 eller 700 bar; Ved 350 bar er tankvolumet målt i energiinnhold en faktor 10 større enn med bensin.
- Væskelagring ved en temperatur på -253 grader (kryogen lagring), hvor tankvolumet med tanke på energiinnhold er en faktor 4 større enn ved bensin. Med gasslagring kan hydrogen lagres på ubestemt tid uten tap av drivstoff eller kompromiss med kvaliteten. Kryogen lagring, derimot, resulterer i dampdannelse. Fordi trykket i tanken øker på grunn av oppvarming, vil hydrogen slippe ut gjennom trykkavlastningsventilen; en lekkasje på ca. to prosent per dag er akseptabelt. Alternative lagringsmuligheter er fortsatt på forskningsstadiet.
Bildet nedenfor viser to lagertanker under bilen. Dette er lagertanker hvor hydrogenet lagres i gassform under et trykk på 700 bar. Disse lagertankene har en veggtykkelse på omtrent 40 millimeter (4 centimeter), noe som gjør dem motstandsdyktige mot høyt trykk.

Nedenfor kan du igjen se hvordan hydrogentankene er montert under bilen. Plastrøret er dreneringen av vann som skapes under konverteringen i brenselcellen.

Fylling med hydrogen:
På tidspunktet for skriving av denne artikkelen er det bare to hydrogenfyllestasjoner i Nederland. En av disse bensinstasjonene er i Rhoon (Sør-Holland). Bildene viser påfyllingsdysene som brukes til å fylle drivstoff. Arbeidstrykket for fylling er 350 bar for nyttekjøretøy og 700 bar for personbiler.


Påfyllingstilkoblingen i bilen er plassert bak den vanlige tankluken. Påfyllingspistolen kobles til denne påfyllingskoblingen. Etter tilkobling av påfyllingsmunnstykket vil tilkoblingen låse seg. Bilens lagertank skal fylles med gassformig hydrogen under et trykk på 700 bar.


Rekkevidde og kostnader for hydrogen
Som et eksempel tar vi en Toyota Mirai (årsmodell 2021) og ser på rekkevidden og tilleggskostnadene:
- Rekkevidde på 650 km;
- Forbruk: 0,84 kg / 100 km;
- Drivstoffpris per km: 0,09 til 13 cent;
- Veiavgift €0,-
Sammenlignet med et kjøretøy med dieselmotor er ikke en brenselcellebil billig. Selv om kostnadene ved veiavgift spiller en stor rolle, er antallet bensinstasjoner i Nederland fortsatt knappe i 2021. Nedenfor er en sammenligning av kostnadene per 100 km med gjeldende drivstoffpriser:
BMW 320d (2012)
- Diesel: € 1,30 per liter;
- Forbruk: 5,8 l/100 km;
- Koster 100 km: €7,54.
Toyota Mirai (2020):
- Hydrogen: €10 per kg;
- Forbruk: 0,84 kg/100km;
- Koster 100 km: €8,40
Relaterte sider:
- Elektrisk drift (Oversikt);
- Energiovergang.
