Soggetti:
- Idrogeno
- Produzione di idrogeno
- Idrogeno come combustibile per un motore Otto
- Cella a combustibile
- Serbatoio di stoccaggio
- Autonomia e costi dell'idrogeno
Idrogeno:
L’idrogeno (chiamato idrogeno in inglese) può essere utilizzato come vettore energetico per alimentare i veicoli. Vettore energetico significa che l'energia è già stata immessa nell'idrogeno in anticipo. Ciò è in contrasto con le fonti energetiche (fossili) come petrolio, gas naturale e carbone, dove l’energia viene ottenuta trasformando queste sostanze bruciandole.
L’idrogeno è quindi qualcosa di completamente diverso dall’iniezione di acqua, che nei motori a benzina non viene utilizzata come vettore energetico, ma esclusivamente per raffreddare la camera di combustione.
L’obiettivo è raggiungere “emissioni zero” con l’idrogeno; una forma di energia che non produce gas nocivi durante l'utilizzo. La transizione dai combustibili fossili alla propulsione elettrica in combinazione con l'idrogeno e una cella a combustibile rientra nell'ambito del transizione energetica. L’alimentazione dei veicoli con l’idrogeno può essere effettuata in due modi diversi:
- Utilizzo dell'idrogeno come carburante per il motore Otto. L'idrogeno sostituisce la benzina.
- Generare energia elettrica utilizzando l’idrogeno in una cella a combustibile. Utilizzando questa energia elettrica, il motore elettrico guiderà il veicolo in modo completamente elettrico.
Entrambe le tecniche sono descritte in questa pagina.
L’idrogeno può essere prodotto con energia sostenibile o basata su combustibili fossili. Cerchiamo di prevenire il più possibile quest’ultimo, perché in futuro i combustibili fossili diventeranno scarsi. La CO2 verrà prodotta anche durante la lavorazione dei combustibili fossili.

Le colonne sottostanti mostrano il contenuto energetico di una batteria, idrogeno e benzina. Vediamo che c'è molto
Batteria:
- Contenuto energetico: 220Wh/kg, 360 Wh/l
- Molto efficiente
- Stoccaggio breve
- Possibilità di rilascio diretto dell'energia
- Il trasporto è complicato
Idrogeno (700 bar):
- Contenuto energetico: 125.000 kJ/kg, 34,72 kWh/kg
- 30% calore, 70% H2 (cella a combustibile PEM)
- Possibilità di stoccaggio prolungato
- Conversione necessaria
- Facile da trasportare
Benzina:
- Valore energetico: 43.000 kJ/kg, 11,94 kWh/kh
- Rendimento fino al 33%
- Possibilità di stoccaggio prolungato
- Conversione necessaria (combustione)
- Facile da trasportare
L’idrogeno si trova ovunque intorno a noi, ma mai gratuitamente. È sempre vincolato. Lo produrremo, lo isoleremo e lo conserveremo.
- 1 kg di gas idrogeno puro (H2) = 11.200 litri a pressione atmosferica
- L'H2 è più piccolo di qualsiasi altra molecola
- L'H2 è più leggero di qualsiasi altra molecola
- H2 è sempre alla ricerca di connessioni
Oltre alla produzione e all'applicazione dell'idrogeno nelle autovetture, questa pagina tratta anche del suo stoccaggio e trasporto (in fondo alla pagina).
Produzione di idrogeno:
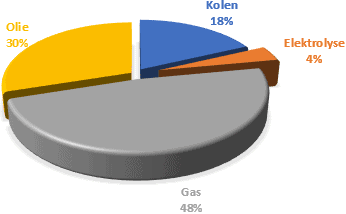
L'idrogeno è un gas che non viene estratto dal suolo, come il gas naturale. L'idrogeno deve essere prodotto. Ciò avviene, tra l'altro, attraverso l'elettrolisi, un processo in cui l'acqua viene convertita in idrogeno e ossigeno. Questa è la reazione inversa che avviene in una cella a combustibile. Inoltre, l’idrogeno può essere ottenuto attraverso processi meno rispettosi dell’ambiente. I dati seguenti mostrano come l’idrogeno potrà essere prodotto nel 2021.
- Carbone: C + H20 -> CO2 + H2 + Nox + SO2 + … (temp: 1300C-1500C)
- Gas naturale: CH4 + H2O -> CO2 + 3H2 (temperatura richiesta: 700°C-1100°C)
- Olio: CxHyNzOaSb + …. -> cH2 + moltissimi sottoprodotti
- Elettrolisi dall'acqua: 2H2O -> 2H2 + O2
L’elettrolisi dell’acqua è molto pulita ed è la forma più rispettosa dell’ambiente di produzione di idrogeno. Questo rilascia idrogeno e ossigeno, a differenza della lavorazione dei combustibili fossili, che rilascia CO2.
- Elettrolisi dell'acqua; L'elettrolisi è una reazione chimica che divide le molecole d'acqua per creare idrogeno e ossigeno puri. L’idrogeno può essere prodotto ovunque ci siano acqua ed elettricità. Uno svantaggio è che è necessaria l’elettricità per produrre idrogeno e poi trasformarlo nuovamente in elettricità. Durante questo processo si perde fino al 50%. Il vantaggio è che l’energia è immagazzinata nell’idrogeno.
- Conversione dei combustibili fossili; petrolio e gas contengono molecole di idrocarburi costituite da carbonio e idrogeno. L’idrogeno può essere separato dal carbonio utilizzando un cosiddetto processore di carburante. Lo svantaggio è che il carbonio scompare nell’aria sotto forma di anidride carbonica.
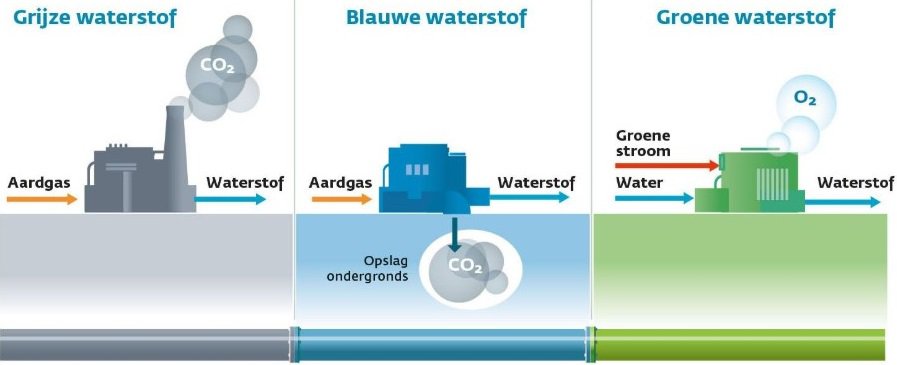
La produzione di idrogeno ottenuta con combustibili fossili è chiamata idrogeno grigio. Questo rilascia NOx e CO2 nell'atmosfera.
Dal 2020 in poi la produzione diventerà sempre più “blu”: la CO2 verrà catturata.
L’obiettivo è produrre esclusivamente idrogeno verde entro il 2030: elettricità verde e acqua sono le fonti per generare l’idrogeno più rispettoso dell’ambiente.
Nel mondo chimico, l'idrogeno è indicato come H2, il che significa che una molecola di idrogeno è composta da due atomi di idrogeno. L'H2 è un gas che non si trova in natura. La molecola H2 è presente in tutti i tipi di sostanze, la più conosciuta è l'acqua (H20). L'idrogeno deve essere ottenuto separando la molecola di idrogeno, ad esempio, da una molecola d'acqua.
Produrre idrogeno attraverso l’elettrolisi è quindi il futuro.
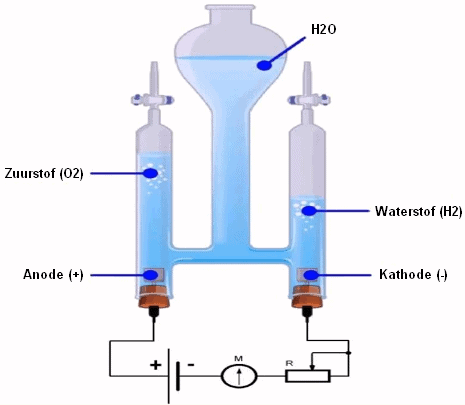
L'immagine seguente mostra un modello comunemente utilizzato nelle lezioni di chimica.
- Le barre positive e negative di una batteria pendono nell'acqua;
- Dal lato dell'anodo si ottiene l'ossigeno;
- Dal lato del catodo si ottiene l'idrogeno.
L'idrogeno prodotto da combustibili fossili, ad esempio metano (CH4), viene in questo caso convertito in H2 e CO2 tramite reforming. La CO2 può essere separata e immagazzinata nel sottosuolo, ad esempio in un giacimento di gas naturale vuoto. L'utilizzo del gas naturale contribuisce quindi in misura minima o nulla alle emissioni di CO2 nell'atmosfera. L’idrogeno può essere ricavato anche dalla biomassa. Se anche la CO2 rilasciata durante questo processo viene separata e immagazzinata nel sottosuolo, è possibile ottenere emissioni di CO2 addirittura negative; rimuovendo la CO2 dall’atmosfera e immagazzinando questa CO2 sulla Terra.
L’idrogeno, a differenza dei combustibili fossili come petrolio, gas naturale e carbone, non è una fonte di energia, ma un vettore energetico. Ciò significa che l’energia rilasciata quando si utilizza l’idrogeno, ad esempio come carburante in un’auto, deve essere prima immessa. L’elettricità è necessaria per produrre idrogeno attraverso l’elettrolisi. La sostenibilità di questo idrogeno dipende quindi in gran parte dalla sostenibilità dell’elettricità utilizzata.
Idrogeno come carburante per un motore Otto:
Un motore Otto è un altro nome per un motore a benzina. Il motore a benzina fu inventato nel 1876 da Nikolaus Otto. In questo caso lo chiamiamo motore Otto, perché la benzina viene sostituita da un altro combustibile, ovvero l'idrogeno. In un motore in cui viene iniettato l'idrogeno non è più presente il serbatoio del carburante con la benzina.
Quando l'idrogeno viene bruciato, non vengono prodotti gas CO2, a differenza dei tradizionali motori Otto e diesel, ma solo acqua. Quando l'idrogeno viene iniettato tramite iniezione diretta, si verifica un aumento di potenza dal 15 al 17% rispetto alla benzina. Quando l'idrogeno viene iniettato nella valvola di aspirazione (iniezione indiretta), avviene un rapido riscaldamento attraverso l'aria. Anche l'aria viene spostata dall'idrogeno. In entrambi i casi nella camera di combustione affluisce meno ossigeno (O2). Nel peggiore dei casi si verifica una perdita di potenza fino al 50%.
Il rapporto tra aria e idrogeno non è così preciso come, ad esempio, nel caso di una miscela aria-benzina. La forma della camera di combustione non ha quindi grande importanza.
L’idrogeno può essere iniettato in due modi:
– Liquido: con una fornitura liquida di idrogeno, la temperatura di combustione scenderà relativamente a causa dell'evaporazione, in modo che si creino meno NOx.
– Gassoso: se l'idrogeno è immagazzinato in forma liquida nel serbatoio e fluisce nello spazio di combustione a temperatura ambiente, è necessario utilizzare un evaporatore per convertire l'idrogeno dallo stato liquido a quello gassoso. In tal caso l'evaporatore viene riscaldato dal liquido di raffreddamento del motore. Le possibili misure per ridurre gli NOx sono; applicando EGR, iniezione d'acqua o uno inferiore rapporto di compressione.
L'immagine seguente mostra quattro situazioni con tre diverse versioni di iniezione di idrogeno. Nella seconda immagine da sinistra, l'idrogeno gassoso viene iniettato indirettamente nel collettore di aspirazione. L'idrogeno gassoso viene riscaldato dalla temperatura ambiente. Inoltre l'idrogeno occupa spazio, facendo fluire meno ossigeno nel cilindro. Questa è la situazione in cui si verifica la maggiore perdita di potenza.
Nella terza immagine l'idrogeno viene fornito in forma liquida. Criogenico significa che l'idrogeno è stato raffreddato molto fortemente (un metodo per immagazzinare grandi quantità di idrogeno in forma liquida in un serbatoio di stoccaggio relativamente piccolo). Poiché la temperatura dell'idrogeno è più bassa e si trova allo stato liquido, avviene un migliore riempimento del cilindro. Grazie alla bassa temperatura si ottiene un rendimento quasi pari a quello di un motore con iniezione diretta (di idrogeno). Il motore a iniezione diretta può essere visto nella quarta immagine. L'intero spazio di combustione è pieno di ossigeno. Quando la valvola di aspirazione è chiusa e il pistone comprime l'aria, una certa quantità di idrogeno viene iniettata attraverso l'iniettore. La candela su questo motore è dietro o accanto all'iniettore (non è mostrata nell'immagine).
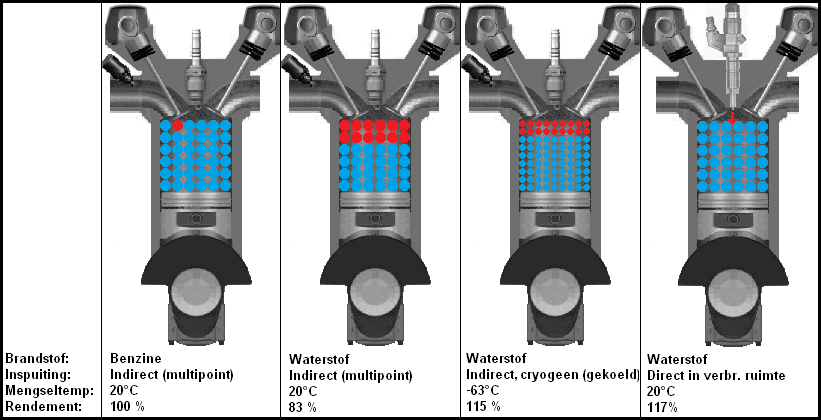
L'efficienza di un motore Otto ovviamente non è del 100%, ma in questa immagine l'efficienza della combustione dell'idrogeno viene confrontata con quella della combustione della benzina.
L’idrogeno ha un’elevata densità di energia per unità di massa (120 MJ/kg), che lo rende quasi tre volte più alta della benzina. Le buone proprietà di accensione dell'idrogeno rendono possibile un funzionamento del motore molto magro, con un valore lambda compreso tra 4 e 5. Lo svantaggio dell'utilizzo di una miscela magra è che la potenza sarà inferiore e le caratteristiche di guida saranno ridotte. Per compensare ciò, viene spesso utilizzata la sovralimentazione (turbo).
A causa dell'area di accensione più ampia rispetto alla benzina, il rischio di detonazione o ritorno di fiamma è maggiore. È quindi molto importante che vi sia un buon controllo dell'alimentazione del carburante e dell'accensione. A pieno carico la temperatura nella camera di combustione può diventare molto elevata. C'è spesso iniezione d'acqua necessario per garantire un raffreddamento sufficiente e quindi anche per evitare un'accensione prematura (sotto forma di detonazione o ritorno di fiamma).
Cella a combustibile:
La sezione precedente ha spiegato come l’idrogeno può fungere da carburante per il motore a combustione. Un'altra applicazione dell'idrogeno è nelle celle a combustibile. Un veicolo dotato di cella a combustibile non ha un motore a combustione ma uno o più motori elettrici. L'energia elettrica per azionare i motori elettrici è prodotta dalla cella a combustibile. Una cella a combustibile è un dispositivo elettrochimico che converte l'energia chimica direttamente in energia elettrica, senza perdite termiche o meccaniche. La conversione dell'energia nella cella a combustibile è quindi molto efficiente. La cella a combustibile generalmente funziona con idrogeno, ma è possibile utilizzare anche un combustibile come il metanolo.
In linea di principio una cella a combustibile può essere paragonata a una batteria, perché entrambe producono elettricità attraverso un processo chimico. La differenza è che l'energia immagazzinata nella batteria viene rilasciata una volta. L'energia si esaurisce nel tempo, quindi la batteria deve essere ricaricata. Una cella a combustibile fornisce energia continua finché i reagenti vengono forniti alla cella elettrochimica. I reagenti sono sostanze chimiche che reagiscono tra loro in una reazione chimica.
In una cella a combustibile, l'idrogeno e l'ossigeno vengono convertiti in ioni H+ e OH- (particelle cariche). Gli ioni sono separati da una membrana in camere separate della cella a combustibile. La cella a combustibile contiene due elettrodi di carbonio porosi sui quali è applicato un catalizzatore; per l'idrogeno (H) un elettrodo negativo (anodo) e per l'ossigeno (O) un elettrodo positivo (catodo).
Gli ioni H+ e OH- vengono condotti l'uno verso l'altro tramite gli elettrodi (anodo e catodo), dopodiché gli ioni + e – reagiscono tra loro. Il catodo catalizza la reazione in cui gli elettroni e i protoni reagiscono con l'ossigeno per formare il prodotto finale due, ovvero l'acqua. Gli ioni H+ e OH- insieme formano una molecola H2O. Questa molecola non è uno ione perché la sua carica elettrica è neutra. La particella più e la particella meno insieme danno una particella neutra.
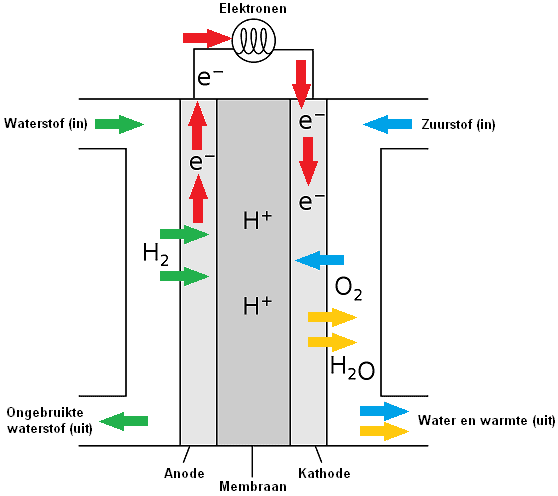
All'anodo avviene l'ossidazione dell'idrogeno (H). L'ossidazione è il processo in cui una molecola dona i suoi elettroni. L'anodo agisce come un catalizzatore, dividendo l'idrogeno in protoni ed elettroni.
La riduzione avviene al catodo aggiungendo ossigeno (O). Gli elettroni, sigillati dall'anodo, viaggeranno verso il catodo tramite un filo elettrico che collega gli elettroni all'esterno.
Non trasferendo gli elettroni direttamente, ma attraverso un percorso esterno (il filo della corrente), questa energia viene in gran parte rilasciata come energia elettrica. Il circuito è chiuso da ioni in un elettrolita di collegamento tra il riduttore e l'ossidante.
La particella che assorbe gli elettroni è chiamata ossidante e viene quindi ridotta. L'agente riducente perde elettroni e si ossida. Una riduzione è il processo mediante il quale una particella assorbe elettroni. Ossidazione e riduzione vanno sempre insieme. Il numero di elettroni rilasciati e assorbiti è sempre lo stesso.
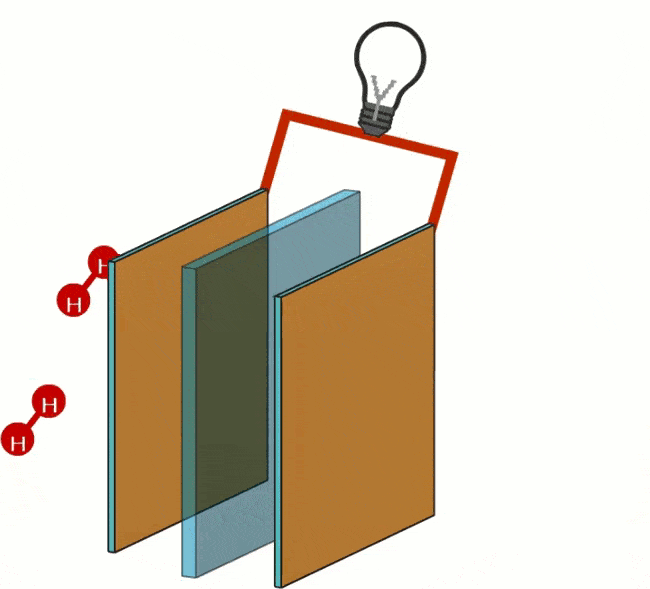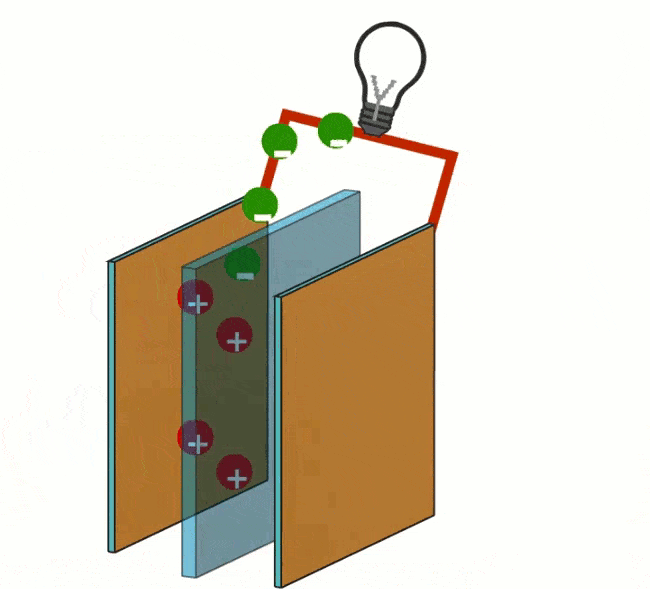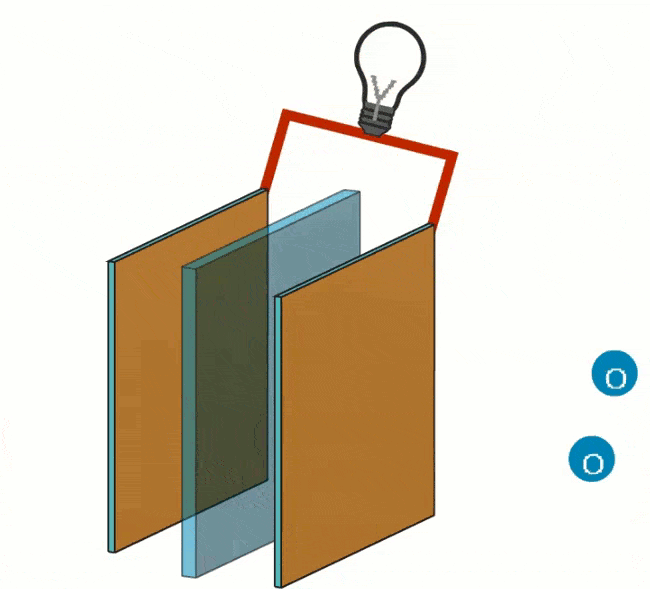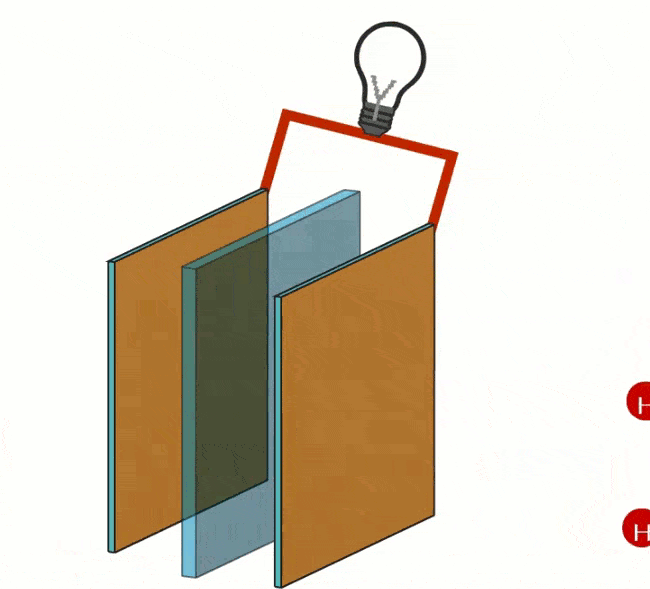
Al polo negativo avviene la seguente reazione:
Al polo positivo avviene una reazione diversa:
L'immagine sotto mostra la vista dal basso di uno stack di celle a combustibile Toyota. Questo stack di celle a combustibile si trova sotto il cofano dell'auto. Il motore elettrico è collegato a questa pila. Il motore elettrico fornisce la potenza alla trasmissione, che è collegata agli alberi di trasmissione per trasmettere le forze motrici alle ruote.
Nella parte superiore della pila si possono vedere diversi tubi dell'aria. Ciò include, tra le altre cose, la pompa dell'aria che pompa l'aria alle celle a combustibile, a seconda della potenza richiesta dal motore elettrico.
Questo stack di celle a combustibile è dotato di 370 celle a combustibile. Ciascuna cella a combustibile fornisce 1 volt, quindi è possibile fornire un totale di 370 volt al motore elettrico. Le celle a combustibile si trovano tutte una sotto l'altra. Il cerchio rosso mostra un ingrandimento dove è chiaramente visibile la sovrapposizione delle celle a combustibile.

Serbatoio di stoccaggio:
Anche se l’idrogeno ha un’elevata densità di energia per unità di massa (120 MJ/kg) ed è quindi quasi tre volte più alta della benzina, la densità di energia per unità di volume è molto bassa a causa della sua massa specifica inferiore. Per lo stoccaggio ciò significa che l'idrogeno deve essere immagazzinato sotto pressione o in forma liquida per poter utilizzare un serbatoio di stoccaggio con un volume gestibile. Esistono due varianti per le applicazioni sui veicoli:
- Stoccaggio gassoso a 350 o 700 bar; A 350 bar il volume del serbatoio in termini di contenuto energetico è 10 volte maggiore rispetto alla benzina.
- Stoccaggio di liquidi a una temperatura di -253 gradi (stoccaggio criogenico), dove il volume del serbatoio in termini di contenuto energetico è 4 volte maggiore rispetto alla benzina. Con lo stoccaggio gassoso, l’idrogeno può essere immagazzinato a tempo indeterminato senza perdite di carburante o compromessi sulla qualità. Lo stoccaggio criogenico, invece, provoca la formazione di vapore. Poiché la pressione nel serbatoio aumenta a causa del riscaldamento, l'idrogeno fuoriesce attraverso la valvola limitatrice di pressione; è accettabile una perdita di circa il XNUMX% al giorno. Opzioni di stoccaggio alternative sono ancora in fase di ricerca.
L'immagine sotto mostra due serbatoi di stoccaggio sotto l'auto. Si tratta di serbatoi di stoccaggio dove l'idrogeno viene immagazzinato in forma gassosa ad una pressione di 700 bar. Questi serbatoi di stoccaggio hanno uno spessore delle pareti di circa 40 millimetri (4 centimetri), che li rende resistenti all'alta pressione.

Qui sotto potete vedere ancora come sono montati i serbatoi dell'idrogeno sotto la vettura. Il tubo in plastica è lo scarico dell'acqua che si crea durante la conversione nella cella a combustibile.

Rifornimento con idrogeno:
Al momento della stesura di questo articolo, nei Paesi Bassi ci sono solo due stazioni di rifornimento di idrogeno. Una di queste stazioni di servizio si trova a Rhoon (Olanda meridionale). Le immagini mostrano gli ugelli di riempimento utilizzati per il rifornimento di carburante. La pressione di esercizio per il riempimento è di 350 bar per i veicoli commerciali e di 700 bar per le autovetture.


Il raccordo di rifornimento nell'auto si trova dietro il solito sportello del carburante. A questo raccordo di riempimento è collegata la pistola di riempimento. Dopo aver collegato l'ugello di riempimento, la connessione si bloccherà. Il serbatoio dell'auto sarà riempito con idrogeno gassoso a una pressione di 700 bar.


Autonomia e costi dell'idrogeno
Ad esempio, prendiamo una Toyota Mirai (anno modello 2021) e osserviamo l'autonomia e i costi aggiuntivi:
- Autonomia di 650 km;
- Consumo: 0,84 kg/100 km;
- Prezzo carburante al km: da 0,09 a 13 centesimi;
- Tassa di circolazione €0,-
Rispetto a un veicolo con motore diesel, un’auto a celle a combustibile non è economica. Sebbene i costi della tassa di circolazione svolgano un ruolo importante, nel 2021 il numero di stazioni di servizio nei Paesi Bassi è ancora scarso. Di seguito è riportato un confronto dei costi per 100 km con i prezzi attuali del carburante:
BMW 320d (2012)
- Diesel: 1,30€ al litro;
- Consumo: 5,8 l/100 km;
- Costo 100 km: 7,54 €.
Toyota Mirai (2020):
- Idrogeno: 10€ al kg;
- Consumo: 0,84 kg/100 km;
- Costo 100 km: 8,40€
Pagine correlate:
- Propulsione elettrica (Panoramica);
- Transizione energetica.
