Thèmes:
- Préface
- Processus circulaire
- Journal du pH
- Comparez le R134a avec le R1234yf
Préface:
Le processus de refroidissement de la climatisation d'une voiture utilise des changements dans l'état d'une substance. Lors d’un changement d’état, comme le passage du liquide à la vapeur, la structure moléculaire de la substance change, ce qui nécessite de la chaleur. La chaleur est absorbée lorsque le liquide se transforme en vapeur, et dans le cas contraire, lors du passage de la vapeur au liquide, de la chaleur est libérée.
Si nous examinons le transfert de chaleur vers et depuis l'environnement, nous constatons que pendant le processus d'évaporation, l'environnement se refroidit, tandis que de la chaleur est libérée et que l'environnement se réchauffe lors de la condensation. Ce refroidissement de l'environnement se produit dans l'évaporateur, tandis que le chauffage a lieu dans le condenseur. Ce processus se répète continuellement, c’est pourquoi on l’appelle un processus circulaire.
Sur la page « Introduction à la climatisation », le processus cyclique avec les différents composants de la climatisation est décrit de manière pratique. Sur cette page, nous approfondirons ce processus cyclique à travers le diagramme log pH.
Processus de recyclage :
Avant de montrer un graphique de pH complet, commençons par le processus du cycle de climatisation. Dans ce processus de cycle, nous utilisons le schéma du réfrigérant R134a. Dans ce diagramme, les zones gaz, gaz-liquide et liquide sont distinguées les unes des autres. Le point critique se situe au sommet, à 101 degrés Celsius et une pression de 40 bars. Il s'agit de la température et de la pression maximales auxquelles le réfrigérant est chimiquement stable. Le contenu thermique (enthalpie) est tracé en fonction de la pression sur l’axe des x. Bien que nous l’appelions souvent « graphique du pH », il s’agit en fait d’un « graphique log-pH » en raison de l’échelle logarithmique.
- Au point 1 du diagramme, le compresseur démarre et aspire le réfrigérant de l'évaporateur. La pression est de 2 bars ;
- Le gaz est comprimé de 1 à 2, augmentant la pression et le contenu calorifique. La pression et la température montent jusqu'à 15 bars et 70 degrés Celsius. Le gaz est surchauffé ;
- En raison du dégagement de chaleur dans le condenseur, le contenu calorifique diminue et donc dans un premier temps la température. Le gaz perd sa surchauffe entre les points 2 et 3, faisant chuter la température de 70 à 55 ° C
- Du point 3 au point 4, il y a dégagement de chaleur à température constante. Ici, le gaz est transformé en liquide. La pression reste constante ;
- Un refroidissement supplémentaire provoque une légère surfusion du liquide (de 4 à 5). Le liquide surfondu sous la haute pression de 15 bars atteint un étranglement au point 5 : le capillaire ou détendeur. Ici, la haute pression est séparée de la basse pression. Du compresseur, nous pouvons également dire que la pression de refoulement est séparée de la pression d'aspiration.
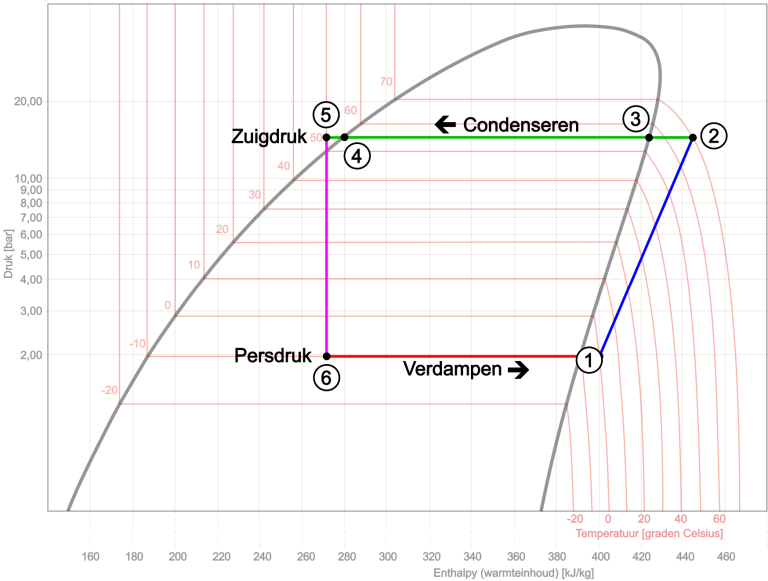
En raison de la chute soudaine de pression dans l’étranglement, le point d’ébullition du réfrigérant en phase liquide diminuera, provoquant une évaporation spontanée. La chaleur nécessaire à cet effet est d'abord extraite du fluide frigorigène lui-même et de son environnement. Cela reste le contenu calorifique est presque constant. Une évaporation complète a alors lieu dans l'évaporateur du point 6 au point 1. La température d'ébullition du réfrigérant chute entre les points 5 et 6 sur 50° C à -10°C, pour finalement se réchauffer jusqu'au point 1 sous forme de gaz à 0°C. Le contenu calorifique du réfrigérant augmente, la chaleur nécessaire étant extraite de l'environnement, en l'occurrence de l'air passant à travers l'évaporateur. La pression et la température restent pratiquement constantes. Le réfrigérant quitte l'évaporateur sous forme de vapeur et est à nouveau aspiré par le compresseur au point 1. Le processus se répète.
Journal du pH :
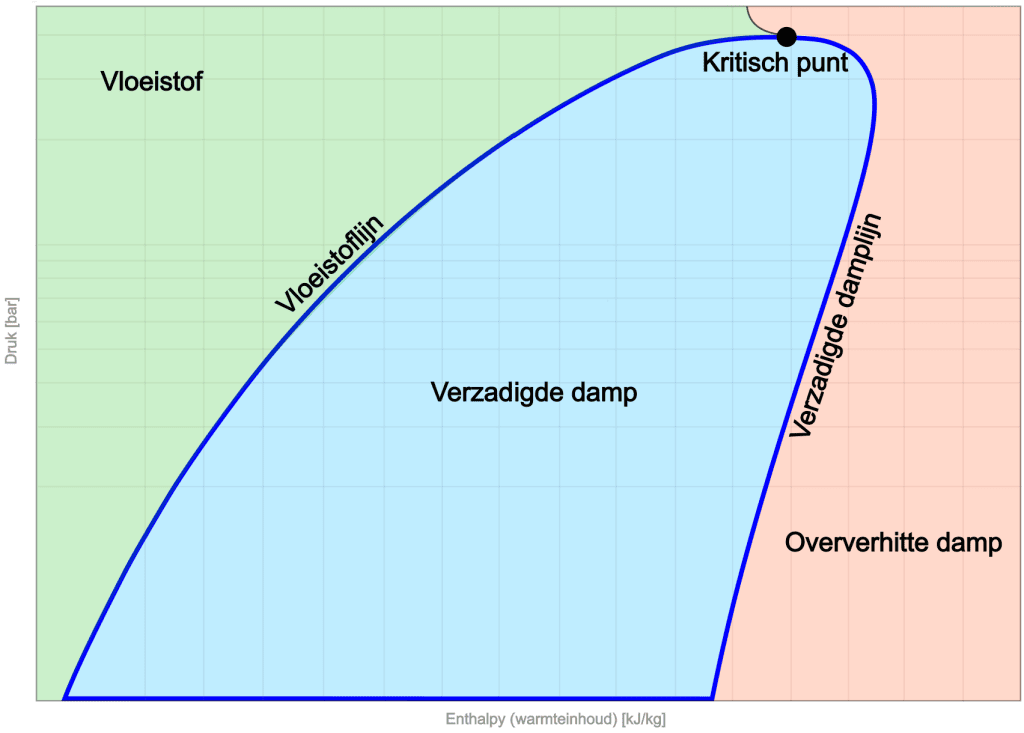
Dans la section précédente, le diagramme log pH a été présenté montrant le processus du cycle (de l'évaporation à la condensation du réfrigérant. L'image ci-dessous montre l'état du réfrigérant à une certaine pression par rapport à l'enthalpie (teneur thermique), dans laquelle le processus de cyclage est indiqué par la ligne bleu foncé.
Sur le côté gauche du diagramme se trouve la zone fluide. À basse enthalpie, le réfrigérant est sous forme liquide. Avec l'augmentation de l'enthalpie, la ligne de liquide est atteinte. La pente de cette ligne indique les changements de pression et d'enthalpie pour la phase liquide.
Au centre du diagramme se trouve la zone de vapeur saturée. Ici, le réfrigérant est en équilibre thermique, avec à la fois du liquide et de la vapeur.
À droite, nous voyons la ligne de vapeur saturée, qui marque la limite à laquelle le réfrigérant s'est complètement évaporé et est en phase vapeur surchauffée.
En haut du diagramme se trouve le point critique, qui marque la frontière entre le liquide et la vapeur. Ici, la distinction entre les phases vapeur et liquide disparaît, laissant le réfrigérant dans un état unique. Il n'y a pas de transition claire entre le liquide et la vapeur.
Pour mieux comprendre le diagramme log-ph, plusieurs courbes sont ajoutées au diagramme ci-dessous : la qualité isentropique, isotherme, isochore et de la vapeur. Dans le dessin ci-dessous, nous voyons à nouveau le processus circulaire (coloré en gris) avec la progression des autres processus. Voici une brève explication de chaque changement d’état :
Isentropique : la ligne et isentropique est caractérisée par une entropie constante. Cela signifie qu'au cours d'un processus de ce type, le réfrigérant n'a aucun échange thermique avec l'environnement et ne subit aucun changement d'entropie. Il s'agit d'une ligne de processus adiabatique efficace (sans échange thermique) dans le diagramme.
Isotherme: Une ligne isotherme dans le diagramme log-pH représente un processus à température constante. Au cours de ce processus, la température du réfrigérant reste constante, ce qui signifie que de la chaleur est fournie ou évacuée pour maintenir le rapport pression-enthalpie (ph) constant.
Isochore : Une ligne isochore dans le diagramme log-pH représente un processus à volume constant. Au cours de ce processus, le volume spécifique du réfrigérant reste constant, ce qui signifie qu'aucun changement de volume ne se produit. Cela permet au style de ligne de monter ou descendre dans le diagramme en fonction d'autres changements tels que la pression et l'enthalpie.
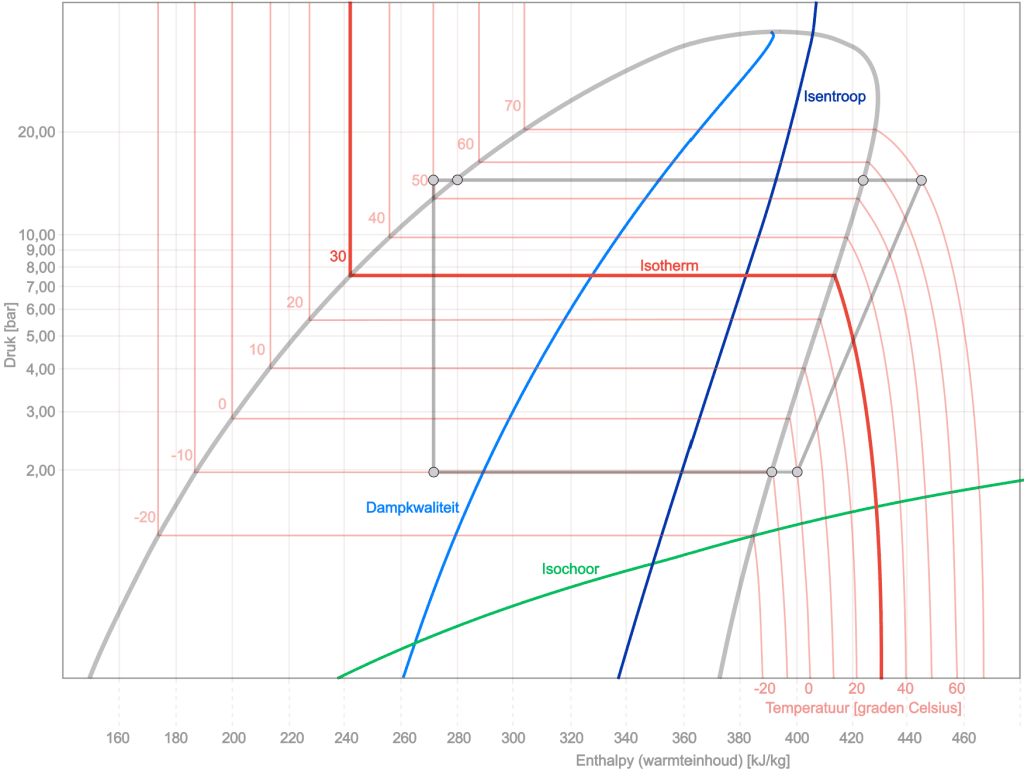
- Qualité de la vapeur : Dans un graphique de pH de réfrigérant, l'axe des x indique la plage de qualité, de « x=0 » (complètement liquide) à « x=1 » (complètement gazeux). Entre ces extrêmes, le réfrigérant est dans un état biphasique, la valeur x indiquant le rapport gaz/liquide. Une ligne allant de « x=0,10 » à « x=0,90 » dans le diagramme indique que le réfrigérant se trouve dans cette plage biphasée, la valeur x spécifique indiquant la répartition gaz/liquide. Ceci est crucial pour comprendre le comportement du réfrigérant dans des applications telles que les systèmes de réfrigération et de climatisation.
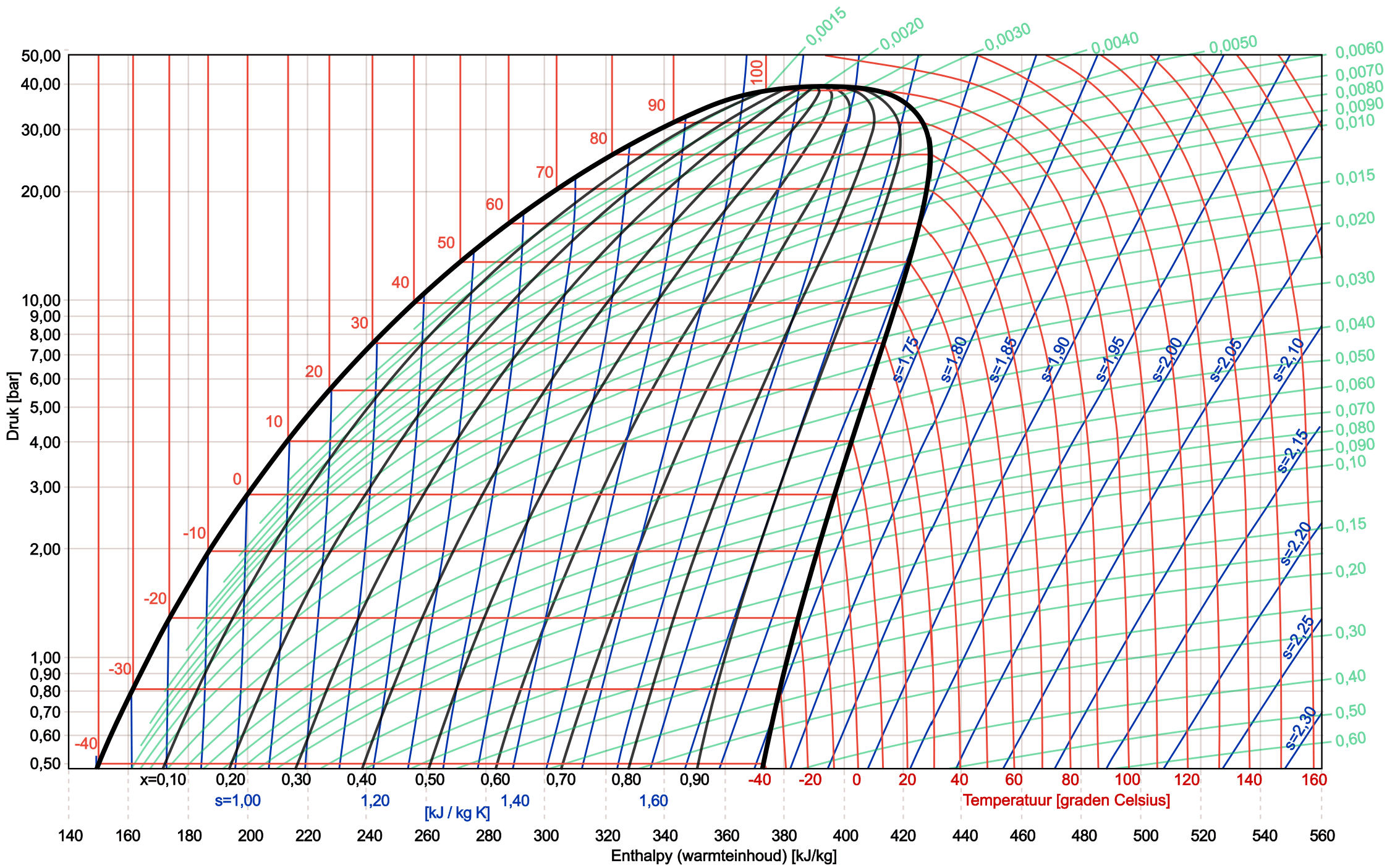
Dans l'image ci-dessous, nous voyons un diagramme logarithmique complet du pH du réfrigérant R134a.
Comparez le R134a avec le R1234yf :
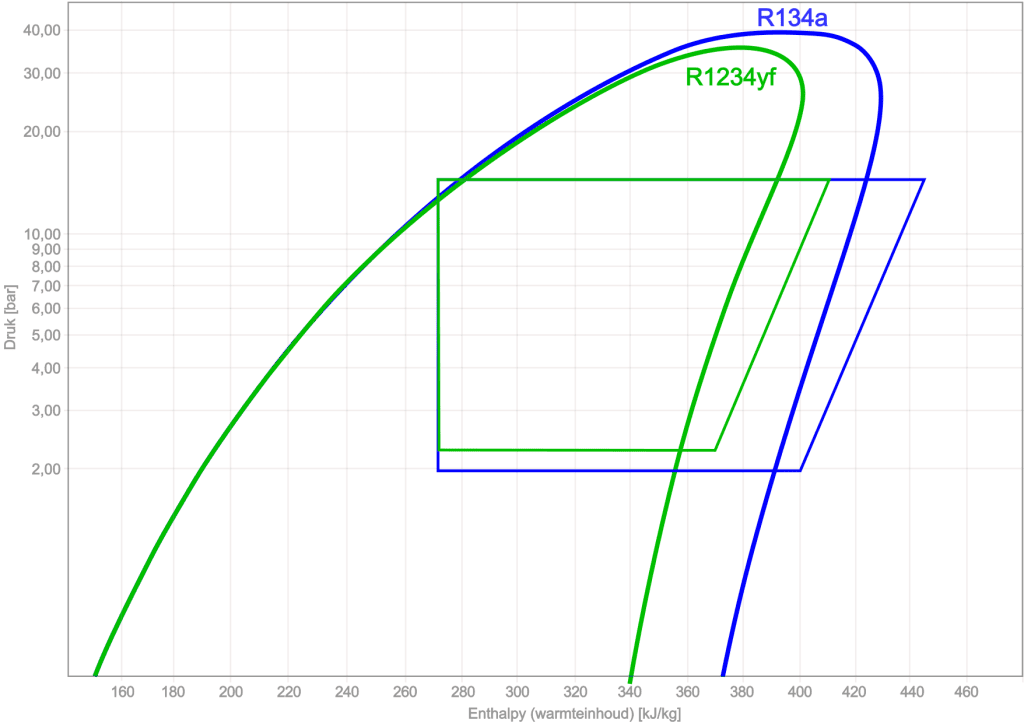
À l’aide du diagramme log pH, différents types de réfrigérants peuvent être comparés les uns aux autres. La figure suivante montre les diagrammes log pH et les processus de cyclage du R134a et du R1234yf.
Page connexe :
