Μαθήματα:
- Εισαγωγή
- Κυκλική διαδικασία
- Διάγραμμα καταγραφής ph
- Συγκρίνετε το R134a με το R1234yf
Εισαγωγή:
Η διαδικασία ψύξης στο κλιματισμό ενός αυτοκινήτου χρησιμοποιεί αλλαγές στην κατάσταση μιας ουσίας. Κατά τη διάρκεια μιας αλλαγής κατάστασης, όπως η μετάβαση από υγρό σε ατμό, η μοριακή δομή της ουσίας αλλάζει, κάτι που απαιτεί θερμότητα. Η θερμότητα απορροφάται όταν το υγρό μετατρέπεται σε ατμό, και στην αντίθετη περίπτωση, κατά τη μετάβαση από ατμό σε υγρό, απελευθερώνεται θερμότητα.
Αν κοιτάξουμε τη μεταφορά θερμότητας προς και από το περιβάλλον, βλέπουμε ότι κατά τη διαδικασία εξάτμισης το περιβάλλον ψύχεται, ενώ απελευθερώνεται θερμότητα και το περιβάλλον θερμαίνεται κατά τη συμπύκνωση. Αυτή η ψύξη του περιβάλλοντος συμβαίνει στον εξατμιστή, ενώ η θέρμανση στον συμπυκνωτή. Αυτή η διαδικασία επαναλαμβάνεται συνεχώς, γι' αυτό και είναι γνωστή ως κυκλική διαδικασία.
Στη σελίδα «Εισαγωγή του κλιματισμού», η διαδικασία κύκλου με τα διάφορα εξαρτήματα του κλιματισμού περιγράφεται με πρακτικό τρόπο. Σε αυτή τη σελίδα θα εμβαθύνουμε περαιτέρω σε αυτή τη διαδικασία κύκλου μέσω του διαγράμματος log pH.
Διαδικασία ανακύκλωσης:
Πριν δείξουμε ένα πλήρες ημερολόγιο pH, ας ξεκινήσουμε με τη διαδικασία του κύκλου κλιματισμού. Σε αυτή τη διαδικασία κύκλου χρησιμοποιούμε το διάγραμμα του ψυκτικού R134a. Σε αυτό το διάγραμμα οι περιοχές για αέριο, αέριο-υγρό και υγρό διακρίνονται μεταξύ τους. Το κρίσιμο σημείο είναι στην κορυφή, στους 101 βαθμούς Κελσίου και πίεση 40 bar. Αυτές είναι η μέγιστη θερμοκρασία και πίεση στην οποία το ψυκτικό μέσο είναι χημικά σταθερό. Η περιεκτικότητα σε θερμότητα (ενθαλπία) απεικονίζεται σε διάγραμμα έναντι της πίεσης στον άξονα x. Αν και συχνά το αναφέρουμε ως "διάγραμμα pH", είναι στην πραγματικότητα ένα "διάγραμμα log-pH" λόγω της λογαριθμικής κλιμάκωσης.
- Στο σημείο 1 του διαγράμματος ξεκινά ο συμπιεστής, ο οποίος αντλεί ψυκτικό από τον εξατμιστή. Η πίεση είναι 2 bar.
- Το αέριο συμπιέζεται από το 1 στο 2, αυξάνοντας την πίεση και την περιεκτικότητα σε θερμότητα. Η πίεση και η θερμοκρασία ανεβαίνουν στα 15 bar και στους 70 βαθμούς Κελσίου. Το αέριο υπερθερμαίνεται.
- Λόγω της απελευθέρωσης θερμότητας στον συμπυκνωτή, η περιεκτικότητα σε θερμότητα μειώνεται και επομένως αρχικά η θερμοκρασία. Το αέριο χάνει την υπερθέρμανση του μεταξύ των σημείων 2 και 3, με αποτέλεσμα η θερμοκρασία να πέσει από τους 70 στους 55 βαθμούς ° C.
- Από το σημείο 3 έως το 4 υπάρχει απελευθέρωση θερμότητας σε σταθερή θερμοκρασία. Εδώ το αέριο μετατρέπεται σε υγρό. Η πίεση παραμένει σταθερή.
- Περαιτέρω ψύξη προκαλεί ελαφρά υπερψύξη του υγρού (από 4 έως 5). Το υπερψυγμένο υγρό υπό την υψηλή πίεση των 15 bar φθάνει σε μια συστολή στο σημείο 5: την τριχοειδή ή τη βαλβίδα εκτόνωσης. Εδώ η υψηλή πίεση διαχωρίζεται από τη χαμηλή πίεση. Από τον συμπιεστή μπορούμε επίσης να πούμε ότι η πίεση εκκένωσης διαχωρίζεται από την πίεση αναρρόφησης.
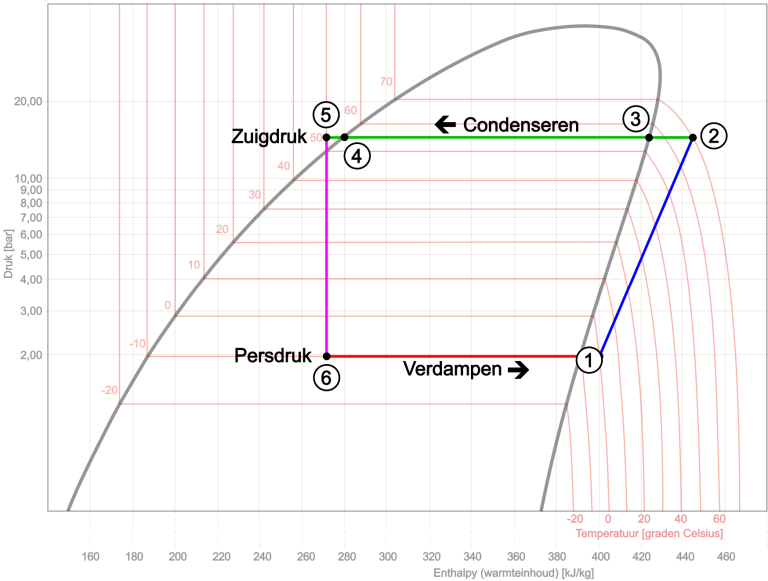
Λόγω της ξαφνικής πτώσης της πίεσης στη στένωση, το σημείο βρασμού του ψυκτικού στην υγρή φάση θα μειωθεί, προκαλώντας αυθόρμητη εξάτμιση. Η θερμότητα που απαιτείται για αυτό εξάγεται πρώτα από το ίδιο το ψυκτικό και το περιβάλλον του. Αυτό παραμένει η περιεκτικότητα σε θερμότητα είναι σχεδόν σταθερή. Στη συνέχεια πραγματοποιείται πλήρης εξάτμιση στον εξατμιστή από το σημείο 6 έως το 1. Η θερμοκρασία βρασμού του ψυκτικού μέσου πέφτει μεταξύ των σημείων 5 και 6 του 50° C στους -10°C, τελικά μέχρι το σημείο 1 ως αέριο στους 0°C. Η θερμική περιεκτικότητα του ψυκτικού μέσου αυξάνεται, με την απαιτούμενη θερμότητα να εξάγεται από το περιβάλλον, στην περίπτωση αυτή ο αέρας που διέρχεται από τον εξατμιστή. Η πίεση και η θερμοκρασία παραμένουν ουσιαστικά σταθερές. Το ψυκτικό εξέρχεται από τον εξατμιστή ως ατμός και αναρροφάται ξανά από τον συμπιεστή στο σημείο 1. Η διαδικασία επαναλαμβάνεται.
Διάγραμμα καταγραφής pH:
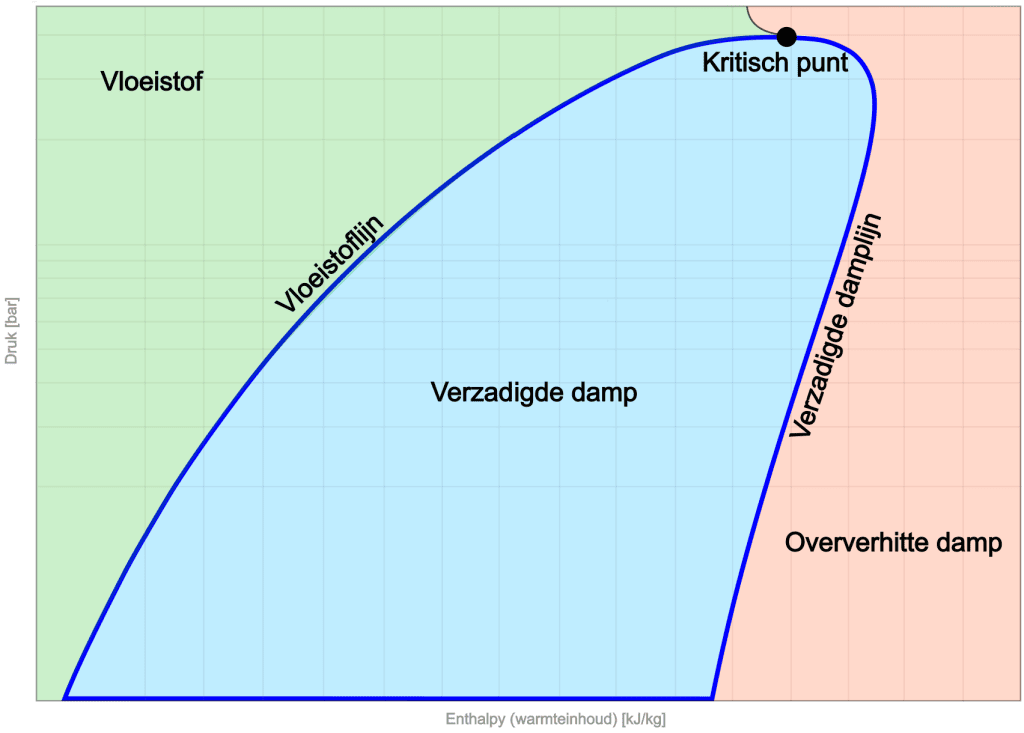
Στην προηγούμενη ενότητα, παρουσιάστηκε το διάγραμμα log pH που δείχνει τη διαδικασία του κύκλου (από την εξάτμιση έως τη συμπύκνωση του ψυκτικού. Η παρακάτω εικόνα δείχνει την κατάσταση του ψυκτικού μέσου σε μια ορισμένη πίεση σε σχέση με την ενθαλπία (περιεκτικότητα σε θερμότητα), στην οποία η διαδικασία του κύκλου υποδεικνύεται με τη σκούρα μπλε γραμμή.
Στην αριστερή πλευρά του διαγράμματος είναι η περιοχή ρευστού. Σε χαμηλή ενθαλπία το ψυκτικό είναι σε υγρή μορφή. Με την αύξηση της ενθαλπίας επιτυγχάνεται η γραμμή του υγρού. Η κλίση αυτής της γραμμής δείχνει τις αλλαγές στην πίεση και την ενθαλπία για την υγρή φάση.
Στο κέντρο του διαγράμματος είναι η ζώνη κορεσμένων ατμών. Εδώ το ψυκτικό είναι σε θερμική ισορροπία, με παρόντα υγρό και ατμό.
Στα δεξιά βλέπουμε τη γραμμή κορεσμένων ατμών, η οποία σηματοδοτεί το όριο στο οποίο το ψυκτικό μέσο έχει εξατμιστεί πλήρως και βρίσκεται σε φάση υπερθερμασμένου ατμού.
Στην κορυφή του διαγράμματος βρίσκεται το κρίσιμο σημείο, το οποίο σηματοδοτεί το όριο μεταξύ υγρού και ατμού. Εδώ η διάκριση μεταξύ της φάσης ατμού και υγρού εξαφανίζεται, αφήνοντας το ψυκτικό σε μοναδική κατάσταση. Δεν υπάρχει σαφής μετάβαση μεταξύ υγρού και ατμού.
Για περισσότερες πληροφορίες σχετικά με το διάγραμμα log-ph, προστίθενται διάφορες καμπύλες στο παρακάτω διάγραμμα: η ισεντροπική, η ισοθερμική, η ισοχωρική και η ποιότητα των ατμών. Στο παρακάτω σχέδιο βλέπουμε για άλλη μια φορά την κυκλική διαδικασία (χρωματισμένο γκρι) με την πρόοδο των άλλων διεργασιών. Ακολουθεί μια σύντομη εξήγηση για κάθε αλλαγή κατάστασης:
Ισεντροπικό: η και ισεντροπική γραμμή χαρακτηρίζεται από σταθερή εντροπία. Αυτό σημαίνει ότι κατά τη διάρκεια μιας διεργασίας κατά μήκος αυτής της γραμμής το ψυκτικό δεν έχει ανταλλαγή θερμότητας με το περιβάλλον και δεν υφίσταται καμία αλλαγή εντροπίας. Είναι μια αποτελεσματική αδιαβατική (χωρίς ανταλλαγή θερμότητας) γραμμή διεργασίας στο διάγραμμα.
Ισόθερμος γραμμή: Μια ισοθερμική γραμμή στο διάγραμμα log-pH αντιπροσωπεύει μια διαδικασία σταθερής θερμοκρασίας. Κατά τη διάρκεια αυτής της διαδικασίας, η θερμοκρασία του ψυκτικού μέσου παραμένει σταθερή, πράγμα που σημαίνει ότι παρέχεται ή αφαιρείται θερμότητα για να διατηρείται σταθερή η αναλογία πίεσης-ενθαλπίας (ph).
Isochore: Μια ισοχορική γραμμή στο διάγραμμα log-pH αντιπροσωπεύει μια διαδικασία σταθερού όγκου. Κατά τη διάρκεια αυτής της διαδικασίας, ο συγκεκριμένος όγκος του ψυκτικού μέσου παραμένει σταθερός, που σημαίνει ότι δεν υπάρχει αλλαγή στον όγκο. Αυτό επιτρέπει στο στυλ γραμμής να μετακινείται προς τα πάνω ή προς τα κάτω στο διάγραμμα ανάλογα με άλλες αλλαγές όπως η πίεση και η ενθαλπία.
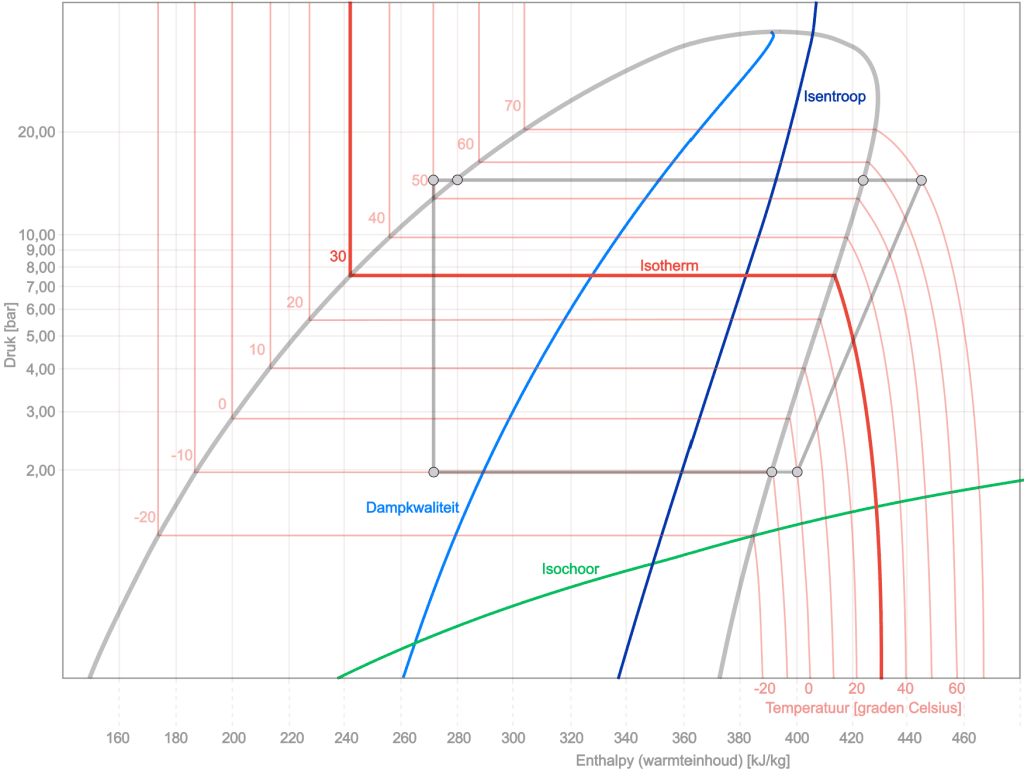
- Ποιότητα ατμού: Σε ένα διάγραμμα log pH ψυκτικού μέσου, ο άξονας x δείχνει το εύρος ποιότητας, από "x=0" (εντελώς υγρό) έως "x=1" (εντελώς αέριο). Μεταξύ αυτών των άκρων, το ψυκτικό είναι σε κατάσταση δύο φάσεων, με την τιμή x να υποδεικνύει την αναλογία αερίου προς υγρό. Μια γραμμή από "x=0,10" έως "x=0,90" στο διάγραμμα υποδεικνύει ότι το ψυκτικό βρίσκεται εντός αυτού του εύρους δύο φάσεων, με τη συγκεκριμένη τιμή x να υποδεικνύει το διαχωρισμό αερίου/υγρού. Αυτό είναι ζωτικής σημασίας για την κατανόηση της συμπεριφοράς του ψυκτικού σε εφαρμογές όπως τα συστήματα ψύξης και κλιματισμού.
Στην παρακάτω εικόνα βλέπουμε ένα πλήρες διάγραμμα log pH του ψυκτικού R134a.
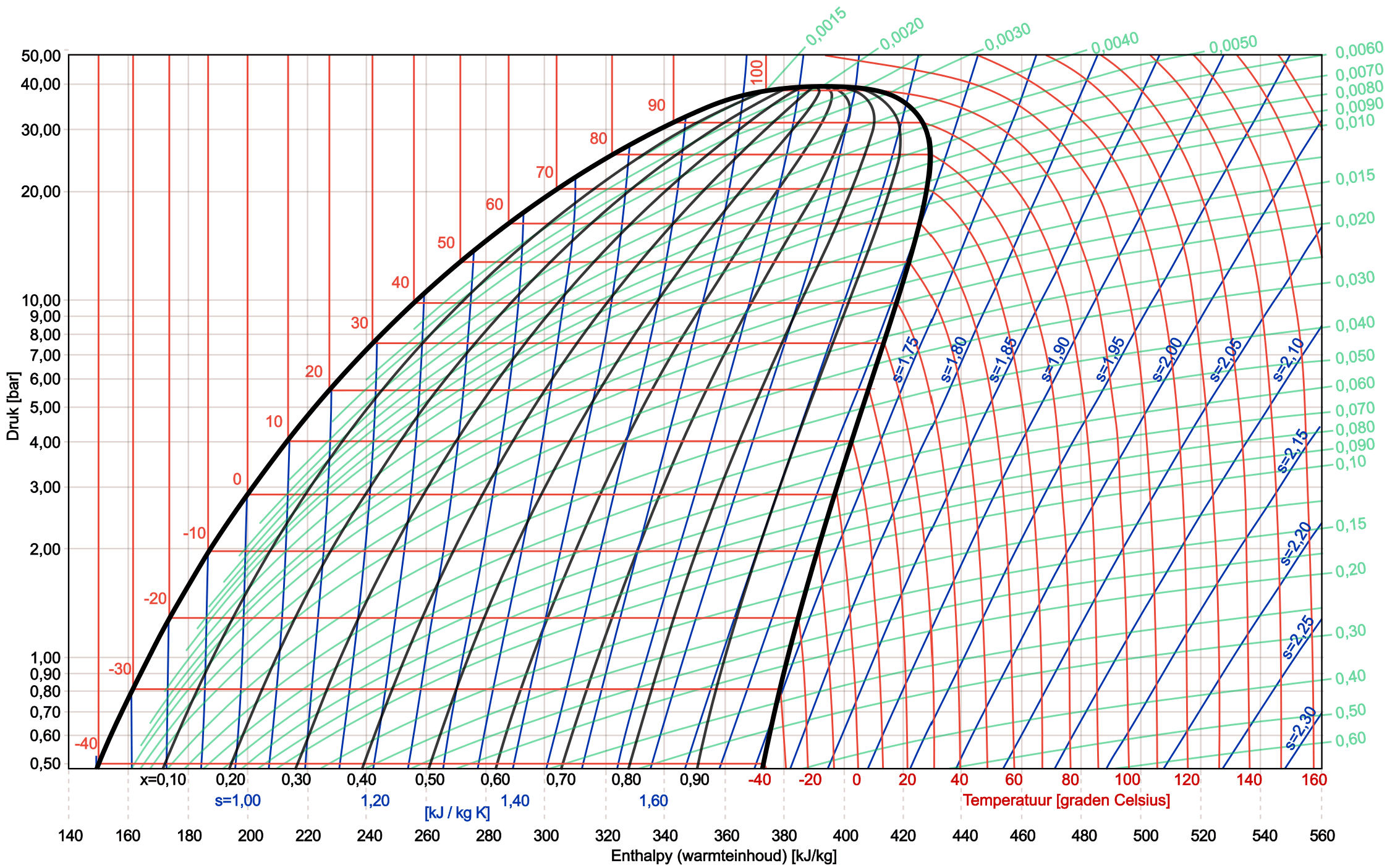
Συγκρίνετε το R134a με το R1234yf:
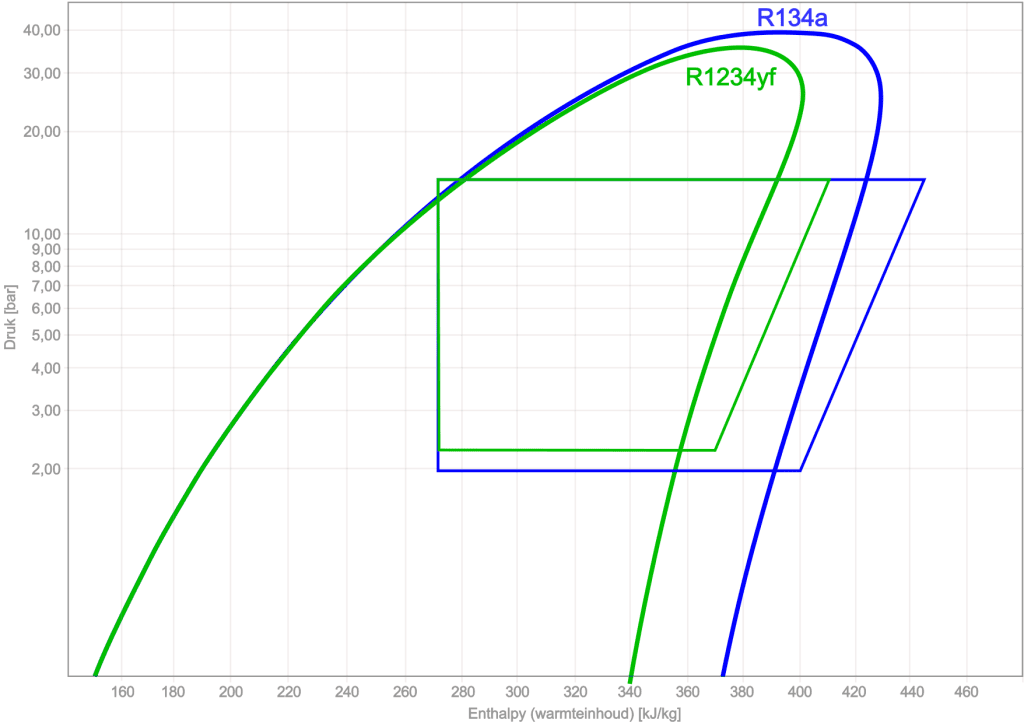
Χρησιμοποιώντας το διάγραμμα log pH, διαφορετικοί τύποι ψυκτικών μπορούν να συγκριθούν μεταξύ τους. Το παρακάτω σχήμα δείχνει τα διαγράμματα log pH και τις διεργασίες ανακύκλωσης των R134a και R1234yf.
Σχετική σελίδα:
